Trong hành trình khám phá vũ trụ hóa học, phản ứng thu nhiệt đóng vai trò là một trong những khái niệm cơ bản, mở ra cánh cửa hiểu biết về cách thức năng lượng được hấp thụ và biến đổi trong các phản ứng hóa học. Trong Bài viết này yeuhohoc.edu.vn sẽ đưa bạn đi từ định nghĩa cơ bản của phản ứng thu nhiệt, qua cơ chế và phân loại, đến việc khám phá ý nghĩa và giá trị của biến thiên enthalpy (ΔH), cuối cùng là cách áp dụng những kiến thức này vào giải quyết các dạng bài tập.
Phản ứng Thu Nhiệt là gì?

Phản ứng thu nhiệt, hay còn gọi là phản ứng hấp thụ nhiệt, là loại phản ứng hóa học mà trong đó năng lượng (thường dưới dạng nhiệt) được hấp thụ từ môi trường xung quanh vào hệ thống phản ứng. Điều này trái ngược với phản ứng tỏa nhiệt, nơi năng lượng được giải phóng.
Phân loại phản ứng thu nhiệt
Dựa vào dạng năng lượng
- Phản ứng thu nhiệt hóa học: Năng lượng được thu nhận dưới dạng nhiệt từ môi trường xung quanh. Ví dụ: phản ứng hòa tan NH4Cl trong nước, phản ứng nung nóng đá vôi.
- Phản ứng thu nhiệt sinh học: Năng lượng được thu nhận dưới dạng năng lượng hóa học từ các phân tử thức ăn. Ví dụ: quá trình quang hợp của thực vật, quá trình hô hấp của tế bào.
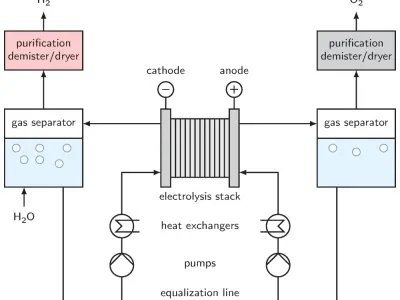
- Phản ứng thu nhiệt vật lý: Năng lượng được thu nhận dưới dạng năng lượng ánh sáng hoặc năng lượng điện. Ví dụ: quá trình ngưng tụ hơi nước, quá trình điện phân nước.
Dựa vào mức độ thu nhiệt
- Phản ứng thu nhiệt mạnh: Phản ứng thu nhận lượng nhiệt lớn, thường có ΔH > 0 kJ/mol. Ví dụ: phản ứng đốt cháy Mg trong khí O2, phản ứng nhiệt nhôm.
- Phản ứng thu nhiệt trung bình: Phản ứng thu nhận lượng nhiệt vừa phải, thường có 0 kJ/mol < ΔH < 50 kJ/mol. Ví dụ: phản ứng hòa tan NaOH trong nước, phản ứng trung hòa axit – bazơ.
- Phản ứng thu nhiệt yếu: Phản ứng thu nhận lượng nhiệt nhỏ, thường có ΔH ≈ 0 kJ/mol. Ví dụ: phản ứng hòa tan KCl trong nước, phản ứng khử SO2 thành H2SO3.
Phân loại theo lĩnh vực
- Phản ứng thu nhiệt trong hóa học: Phản ứng hòa tan, phản ứng trung hòa, phản ứng tổng hợp, phản ứng phân hủy.
- Phản ứng thu nhiệt trong sinh học: Quang hợp, hô hấp tế bào, lên men, cố định nitơ.
- Phản ứng thu nhiệt trong vật lý: Ngưng tụ, hóa rắn, tan chảy, bay hơi.
Lưu ý:
- Phân loại phản ứng thu nhiệt có thể dựa trên nhiều tiêu chí khác nhau.
- Một số phản ứng có thể thuộc nhiều loại phân loại.
Ví dụ:
- Phản ứng hòa tan NH4Cl trong nước là phản ứng thu nhiệt hóa học, thu nhiệt yếu.
- Quá trình quang hợp của thực vật là phản ứng thu nhiệt sinh học, thu nhiệt mạnh.
- Quá trình ngưng tụ hơi nước là phản ứng thu nhiệt vật lý, thu nhiệt trung bình.
Cơ chế của phản ứng thu nhiệt:
Phản ứng thu nhiệt là phản ứng hóa học trong đó năng lượng được hấp thụ từ môi trường xung quanh để phá vỡ các liên kết hóa học trong các chất tham gia, tạo thành các liên kết mới trong các sản phẩm. Năng lượng được hấp thụ này thường ở dạng nhiệt, nhưng cũng có thể ở dạng ánh sáng hoặc năng lượng điện.
Phá vỡ liên kết
- Trong phản ứng thu nhiệt, năng lượng được hấp thụ để phá vỡ các liên kết hóa học giữa các chất tham gia phản ứng.
- Năng lượng liên kết đề cập đến lượng năng lượng cần thiết để giải phóng một liên kết hóa học.
- Các liên kết hóa học trong các chất tham gia thường có năng lượng liên kết cao hơn các liên kết hóa học trong các sản phẩm.
- Do đó, năng lượng cần thiết để phá vỡ các liên kết hóa học trong các chất tham gia lớn hơn năng lượng được giải phóng khi hình thành các liên kết hóa học trong các sản phẩm.
Hình thành liên kết
- Sau khi các liên kết hóa học trong các chất tham gia bị phá vỡ, các nguyên tử và phân tử tự do được tạo thành.
- Các nguyên tử và phân tử tự do này sau đó kết hợp với nhau để tạo thành các liên kết hóa học mới trong các sản phẩm.
- Năng lượng liên kết của các liên kết hóa học mới trong các sản phẩm thường thấp hơn năng lượng liên kết của các liên kết hóa học trong các chất tham gia.
- Do đó, năng lượng được giải phóng khi hình thành các liên kết hóa học mới trong các sản phẩm nhỏ hơn năng lượng cần thiết để phá vỡ các liên kết hóa học trong các chất tham gia.
Chênh lệch năng lượng
- Sự khác biệt về năng lượng liên kết giữa các chất tham gia và sản phẩm là nguyên nhân dẫn đến sự thu nhiệt của phản ứng.
- Năng lượng thu vào (Q) của phản ứng bằng với sự chênh lệch năng lượng giữa các chất tham gia và sản phẩm:

- ΔH° là enthalpy tiêu chuẩn tạo thành của một chất.
- Enthalpy tiêu chuẩn tạo thành của một chất là lượng nhiệt được giải phóng hoặc hấp thụ khi 1 mol chất đó được hình thành từ các nguyên tố ở trạng thái tiêu chuẩn.
Yếu tố ảnh hưởng
- Tốc độ của phản ứng thu nhiệt phụ thuộc vào nhiều yếu tố, bao gồm:
- Tốc độ phản ứng tăng lên khi nhiệt độ tăng cao.
- Chất xúc tác: Chất xúc tác có thể làm giảm năng lượng hoạt hóa của phản ứng, giúp phản ứng xảy ra nhanh hơn.
- Nồng độ: Nồng độ của các chất tham gia càng cao, tốc độ phản ứng càng nhanh.
Ví dụ:
- Phản ứng hòa tan NH4Cl trong nước là một phản ứng thu nhiệt.
- Năng lượng được hấp thụ từ môi trường xung quanh để phá vỡ các liên kết hydro giữa các phân tử NH4Cl và các phân tử nước.
- Sau khi các liên kết hydro bị phá vỡ, các ion NH4+ và Cl- được tạo thành.
- Các ion NH4+ và Cl- sau đó kết hợp với các phân tử nước để tạo thành các liên kết ion mới.
- Năng lượng liên kết của các liên kết ion mới trong dung dịch NH4Cl thấp hơn năng lượng liên kết của các liên kết hydro giữa các phân tử NH4Cl và các phân tử nước.
- Do đó, phản ứng hòa tan NH4Cl trong nước là một phản ứng thu nhiệt.
Biến thiên enthalpy chuẩn của phản ứng
Biến thiên enthalpy chuẩn của phản ứng (ΔrH0) là lượng nhiệt được tỏa ra hoặc hấp thụ khi 1 mol phản ứng xảy ra hoàn toàn ở điều kiện chuẩn (1 atm áp suất, 25°C).
Dấu hiệu của ΔrH0:
- ΔrH0 > 0: Phản ứng thu nhiệt, hệ thống hấp thụ nhiệt từ môi trường xung quanh.
- ΔrH0 < 0: Phản ứng tỏa nhiệt, hệ thống tỏa nhiệt ra môi trường xung quanh.
Cách tính ΔrH0:
- Phương pháp 1: Dùng nhiệt tạo thành chuẩn
ΔrH0 = ΣΔfH0(sản phẩm) – ΣΔfH0(chất tham gia)
- ΔfH0: Enthalpy tạo thành chuẩn của một chất.
- Enthalpy tạo thành chuẩn của một chất là lượng nhiệt được tỏa ra hoặc hấp thụ khi 1 mol chất đó được hình thành từ các nguyên tố ở trạng thái tiêu chuẩn.
- Phương pháp 2: Dùng năng lượng liên kết

- D: Năng lượng liên kết của một liên kết hóa học.
Ví dụ:
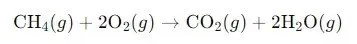 (l)
(l)
ΔrH0 = -890.4 kJ/mol
- Phản ứng này là phản ứng tỏa nhiệt vì ΔrH0 < 0.
- Lượng nhiệt tỏa ra khi 1 mol methane cháy hoàn toàn là 890.4 kJ.
Ứng dụng:
- Dự đoán khả năng xảy ra của phản ứng.
- Tính toán lượng nhiệt cần thiết hoặc tỏa ra trong phản ứng.
- So sánh mức độ tỏa nhiệt hoặc thu nhiệt của các phản ứng khác nhau.
Lưu ý:
- Giá trị ΔrH0 phụ thuộc vào điều kiện phản ứng (áp suất, nhiệt độ).
- Cần sử dụng bảng giá trị enthalpy tạo thành chuẩn hoặc năng lượng liên kết phù hợp với điều kiện phản ứng.
Các dạng bài tập của phản ứng thu nhiệt
Dạng 1: Xác định phản ứng thu nhiệt hay tỏa nhiệt dựa vào dữ kiện đề bài
Ví dụ:
Cho biết phản ứng sau:
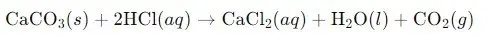
a) Xác định phản ứng trên là thu nhiệt hay tỏa nhiệt.
b) Giải thích dựa vào biến thiên enthalpy của phản ứng.
Lời giải:
a) Cách 1: Dựa vào dấu hiệu của biến thiên enthalpy
- Phản ứng xảy ra trong điều kiện thường: Phản ứng tỏa nhiệt.
- Phản ứng cần đun nóng: Phản ứng thu nhiệt.
Vì phản ứng 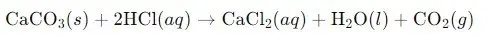 cần đun nóng nên đây là phản ứng thu nhiệt.
cần đun nóng nên đây là phản ứng thu nhiệt.
Cách 2: Dựa vào giá trị enthalpy tạo thành chuẩn
- ΔfH0(CaCO3(r)) = -1206.9 kJ/mol
- ΔfH0(HCl(aq)) = -167.2 kJ/mol
- ΔfH0(CaCl2(aq)) = -795.8 kJ/mol
- ΔfH0(H2O(l)) = -285.8 kJ/mol
- ΔfH0(CO2(g)) = -393.5 kJ/mol
ΔH0 = ΣΔfH0(sản phẩm) – ΣΔfH0(chất tham gia)
= [ΔfH0(CaCl2(aq)) + ΔfH0(H2O(l)) + ΔfH0(CO2(g))] – [ΔfH0(CaCO3(r)) + 2ΔfH0(HCl(aq))]
= (-795.8 kJ/mol – 285.8 kJ/mol – 393.5 kJ/mol) – (-1206.9 kJ/mol – 2 × -167.2 kJ/mol)
= 107.1 kJ/mol
Vì ΔH0 > 0 nên phản ứng thu nhiệt.
b) Giải thích dựa vào biến thiên enthalpy của phản ứng
- Biến thiên enthalpy của phản ứng (ΔH0) là lượng nhiệt tỏa ra hoặc hấp thụ khi 1 mol phản ứng xảy ra hoàn toàn ở điều kiện chuẩn.
- ΔH0 > 0: Phản ứng thu nhiệt, hệ thống hấp thụ nhiệt từ môi trường xung quanh.
- ΔH0 < 0: Phản ứng tỏa nhiệt, hệ thống tỏa ra nhiệt ra môi trường xung quanh.
Vì ΔH0 của phản ứng CaCO3(r) + 2HCl(aq) → CaCl2(aq) + H2O(l) + CO2(g) là 107.1 kJ/mol, nên phản ứng này thu nhiệt. Hệ thống hấp thụ 107.1 kJ nhiệt từ môi trường xung quanh khi 1 mol phản ứng xảy ra hoàn toàn ở điều kiện chuẩn.
Dạng 2: Tính toán lượng nhiệt cần thiết hoặc tỏa ra trong phản ứng thu nhiệt
Ví dụ:
Cho phản ứng:
(g)
a) Tính lượng nhiệt cần thiết để đốt cháy 100 mol khí NH3.
b) Giải thích ý nghĩa của giá trị ΔH0
Lời giải chi tiết
a) Tính lượng nhiệt cần thiết để đốt cháy 100 mol khí NH3:
Bước 1: Viết phương trình phản ứng cân bằng:
(g)
Bước 2: Tính biến thiên enthalpy của phản ứng:
- ΔfH0(NH3(g)) = -46.1 kJ/mol
- ΔfH0(N2(g)) = 0 kJ/mol
- ΔfH0(H2(g)) = 0 kJ/mol
ΔH0 = ΣΔfH0(sản phẩm) – ΣΔfH0(chất tham gia)
= [ΔfH0(N2(g)) + 3ΔfH0(H2(g))] – 2ΔfH0(NH3(g))
= [0 kJ/mol + 3 × 0 kJ/mol] – 2 × (-46.1 kJ/mol)
= 92.2 kJ/mol
Bước 3: Tính lượng nhiệt cần thiết:
- n(NH3) = 100 mol
- Q = n(NH3) × ΔH0
= 100 mol × 92.2 kJ/mol
= 9220 kJ
Vậy cần thiết 9220 kJ để đốt cháy 100 mol khí NH3.
b) Giải thích ý nghĩa của giá trị ΔH0:
- ΔH0 = 92.2 kJ/mol > 0
⇒ Phản ứng đốt cháy NH3 là phản ứng thu nhiệt.
- Hệ thống hấp thụ 92.2 kJ nhiệt từ môi trường xung quanh khi 1 mol NH3 cháy hoàn toàn ở điều kiện chuẩn.
Giá trị ΔH0 cho biết:
- Lượng nhiệt tỏa ra hoặc hấp thụ khi 1 mol phản ứng xảy ra hoàn toàn ở điều kiện chuẩn.
- Phản ứng thu nhiệt (ΔH0 > 0) hay tỏa nhiệt (ΔH0 < 0).