Lanthan, nguyên tố đầu tiên trong dãy Lanthanide với số nguyên tử 57, đóng một vai trò không thể thiếu trong công nghệ hiện đại, từ sản xuất điện tử đến chế tạo vật liệu. Với tính chất hóa học đặc biệt và khả năng tương tác mạnh mẽ với các nguyên tố khác, Lanthan là chìa khóa cho nhiều ứng dụng công nghệ cao. Bài viết này, yeuhoahoc.edu.vn sẽ giới thiệu tổng quan về Lanthan, bao gồm cấu trúc, tính chất, và vai trò của nó trong nền kinh tế toàn cầu, mở ra cái nhìn mới mẻ về nguyên tố quan trọng này trong bảng tuần hoàn.
Giới thiệu về nguyên tố Lanthan (Lanthanide)
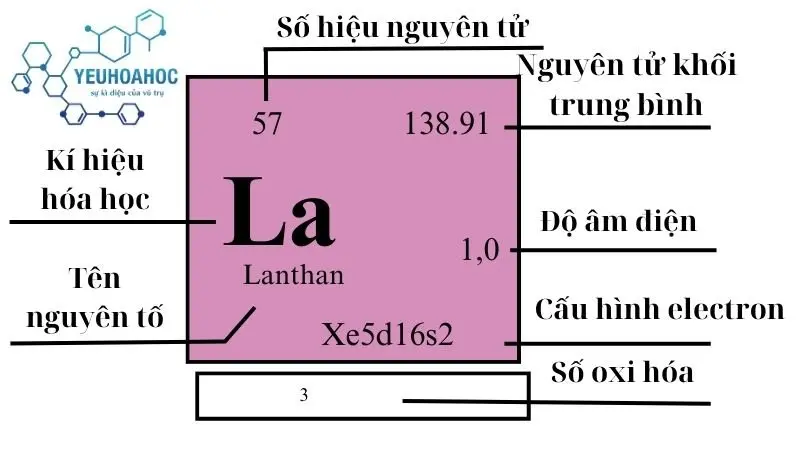
Định nghĩa
Nguyên tố Lanthan, còn được gọi bằng tên tiếng Anh là “Lanthanum”, có kí hiệu là “La” trong bảng tuần hoàn hóa học. Lanthan là một nguyên tố hóa học thuộc nhóm các nguyên tố hiếm, nằm trong nhóm Lanthanide. Lanthanum là một kim loại mềm, có thể cắt được bằng dao, và nó sở hữu một số tính chất vật lý và hóa học đặc trưng giúp nó ứng dụng trong nhiều lĩnh vực như sản xuất thép, sản xuất kính đặc biệt, và trong công nghệ pin.
Lịch sử hình thành nguyên tố Lanthan
1794: Johann Gadolin phát hiện ra Yttria, một khoáng chất chứa các nguyên tố đất hiếm.
1803: Berzelius phân lập được cerium từ Yttria.
1839: Carl Mosander phân lập được Lanthan từ Ceria.
1879: Marc Delafontaine phát hiện ra Samarium.
1907: Georges Urbain phân lập được Gadolinium và Lutetium.
Một số mốc thời gian quan trọng trong lịch sử phát hiện:
- 1839: Carl Mosander phát hiện ra Lanthan, nguyên tố đầu tiên trong nhóm Lanthan.
- 1907: Georges Urbain hoàn thành việc khám phá nhóm Lanthan với Luteti.
- 1945: Glenn Seaborg và cộng sự phát hiện ra Promethium, nguyên tố nhân tạo đầu tiên trong nhóm Lanthan.
Nguyên tố Lanthan trong bảng tuần hoàn hóa học
- Thuộc nhóm 3 (kim loại chuyển tiếp)
- Chu kỳ 6
- Khối lượng nguyên tử: từ 138,905452 u (Lanthan) đến 175,043 u (Luteti)
| Nhóm | Chu kỳ | Nguyên tử khối (u) | Khối lượng riêng g/cm3 | Nhiệt độ nóng chảy (K9) | Nhiệt độ bay hơi K | Nhiệt dung riêng J/g.K | Độ âm điện | Tỷ lệ trong vỏ Trái Đất mg/kg |
| 6 | 138,90547(7) | 6,145 | 1193 | 3737 | 0,195 | 1,1 | 39 |
Tính chất của nguyên tố Lanthan (Lanthanide)
Tính chất vật lý
- Kim loại màu trắng bạc
- Dễ dát mỏng và kéo sợi
- Điểm nóng chảy và sôi thấp
- Khối lượng riêng cao
- Tính dẫn điện và dẫn nhiệt tốt
Tính chất hóa học
- Hoạt động hóa học cao
- Dễ bị oxy hóa
- Tạo hợp chất với nhiều nguyên tố khác
- Có nhiều trạng thái oxy hóa
- Tính khử mạnh
Một số tính chất đặc trưng:
- Tính khử: Các nguyên tố Lanthan có tính khử mạnh, giảm dần từ trái sang phải trong bảng tuần hoàn.
- Tính bazơ: Các nguyên tố Lanthan có tính bazơ mạnh, tăng dần từ trái sang phải trong bảng tuần hoàn.
- Tính tạo phức: Các nguyên tố Lanthan có khả năng tạo phức với nhiều phối tử khác nhau.
- Tính parama từ: Hầu hết các nguyên tố Lanthan đều có tính parama từ.
Ứng dụng của nguyên tố Lanthan (Lanthanide)

Hợp kim:
- Lanthan được sử dụng để tạo ra các hợp kim có độ bền cao, chống ăn mòn và chịu nhiệt tốt.
- Ví dụ: hợp kim thép Lanthan được sử dụng trong các ứng dụng chịu tải trọng cao như động cơ máy bay và trục xe.
Nam châm:
- Một số nguyên tố Lanthan, như Neodymium và Dysprosium, được sử dụng để tạo ra các nam châm vĩnh cửu mạnh mẽ.
- Nam châm Lanthan được sử dụng trong nhiều ứng dụng khác nhau, bao gồm động cơ điện, máy móc MRI và ổ cứng máy tính.
Laser:
- Một số nguyên tố Lanthan, như Yttrium và Erbium, được sử dụng trong các laser có hiệu suất cao.
- Laser Lanthan được sử dụng trong nhiều ứng dụng khác nhau, bao gồm cắt kim loại, phẫu thuật và thông tin liên lạc.
Y học:
- Một số nguyên tố Lanthan, như Gadolinium và Lutetium, được sử dụng trong các chất tương phản MRI.
- Chất tương phản MRI giúp các bác sĩ nhìn thấy các mô và cơ quan trong cơ thể rõ ràng hơn.
- Các nguyên tố Lanthan khác được sử dụng để điều trị một số bệnh, như loãng xương và bệnh Paget.
Điều chế và sản xuất nguyên tố Lanthan
Điều chế trong phòng thí nghiệm
Trong phòng thí nghiệm, Lanthan có thể được điều chế thông qua quá trình giảm phân cực của các hợp chất của nó, thường là halides, bằng cách sử dụng kim loại hoạt động như Canxi. Phản ứng điển hình để điều chế Lanthan trong phòng thí nghiệm có thể được mô tả như sau:
3Ca+2LaF3→2La+3CaF2
Trong phản ứng này, Canxi hoạt động như một chất khử, phản ứng với Lanthan fluoride (LaF₃) để tạo ra Lanthan kim loại và Canxi fluoride như sản phẩm phụ. Phương pháp này đòi hỏi điều kiện nhiệt độ cao và một hệ thống phản ứng kín để tránh sự oxi hóa của Lanthan kim loại bởi không khí.
Điều chế trong công nghiệp
Quá trình sản xuất Lanthan trong công nghiệp thường bao gồm các bước tách và tinh chế từ các khoáng vật chứa Lanthanide như monazite hoặc bastnäsite. Các khoáng vật này được xử lý để tách các nguyên tố đất hiếm khỏi nhau, thông qua quá trình hòa tan, kết tủa, và sự trao đổi ion.
Một trong những phương pháp điều chế công nghiệp phổ biến là sử dụng phương pháp điện phân của muối Lanthan halide tan trong muối nóng chảy. Phương pháp này sản xuất Lanthan kim loại tinh khiết cao:
La2O3+3C→2La+3CO
Ở đây, Lanthan oxit (La₂O₃) được phản ứng với than cốc trong lò nhiệt độ cao để tạo ra Lanthan kim loại và khí carbon monoxide.
Sản xuất
Sản xuất nguyên tố Lanthan ở quy mô công nghiệp đòi hỏi các bước phức tạp và chi phí cao liên quan đến việc tách, tinh chế, và điều chế từ nguồn khoáng sản. Quá trình bắt đầu từ việc khai thác khoáng sản chứa Lanthanide, tiếp theo là quá trình hòa tan và tách chúng từ các nguyên tố đất hiếm khác.
Sau khi đã tách được Lanthan từ hỗn hợp các nguyên tố đất hiếm, nó được chuyển thành dạng oxit hoặc halide để thực hiện điều chế kim loại. Điện phân muối nóng chảy là một trong những phương pháp chính để thu được Lanthan kim loại tinh khiết từ các hợp chất của nó.
Quy trình sản xuất Lanthan yêu cầu kiểm soát chặt chẽ các điều kiện phản ứng và thiết bị chuyên dụng để đảm bảo hiệu quả và an toàn, đặc biệt là trong các bước nhiệt độ cao như điện phân và phản ứng hóa học. Lanthan và các nguyên tố đất hiếm khác có vai trò quan trọng trong nhiều ứng dụng công nghệ cao, đòi hỏi chất lượng và độ tinh khiết cao của nguyên liệu.
Phản ứng của nguyên tố Lanthan (Lanthanide)
Nguyên tố Lanthan (hay còn gọi là kim loại đất hiếm) có tính khử mạnh và hoạt động hóa học cao, do đó nó có thể phản ứng với nhiều chất khác nhau.
Phản ứng với nước
Lanthan phản ứng mãnh liệt với nước, tạo ra hydro và hydroxit Lanthan:
2La + 6H₂O → 2La(OH)₃ + 3H₂
Phản ứng này tỏa nhiệt mạnh và có thể gây nổ nếu không được kiểm soát cẩn thận.
Phản ứng với axit
Lanthan phản ứng với axit để tạo thành muối và hydro:
2La + 6HCl → 2LaCl₃ + 3H₂
Phản ứng với oxy
Lanthan phản ứng với oxy để tạo thành oxit Lanthan:
4La + 3O₂ → 2La₂O₃
Phản ứng với phi kim
Lanthan phản ứng trực tiếp với hầu hết các phi kim (trừ nitơ) để tạo thành muối:
- Với clo:
2La + 3Cl₂ → 2LaCl₃
- Với brom:
2La + 3Br₂ → 2LaBr₃
- Với iốt:
2La + 3I₂ → 2LaI₃
Phản ứng với dung dịch muối
Lanthan có thể khử các cation kim loại khác trong dung dịch muối:
La + 2AgNO₃ → La(NO₃)₃ + 2Ag
Vấn đề an toàn khi sử dụng nguyên tố Lanthan
Độc hại
Lanthan là kim loại độc hại. Khi tiếp xúc với Lanthan, đặc biệt là qua đường uống hoặc hít phải, nó có thể gây ra các triệu chứng như buồn nôn, nôn mửa, tiêu chảy, yếu cơ, tê bì, và thậm chí tử vong.
Nguy cơ cháy nổ
Lanthan có thể phản ứng mãnh liệt với nước, tạo thành Lanthan hydroxit (La(OH)3) và khí hydro (H2). Khí hydro có thể dễ dàng bốc cháy và gây ra nguy cơ cháy nổ.
Gây kích ứng da và mắt
Lanthan có thể gây kích ứng da và mắt. Khi tiếp xúc với Lanthan, cần rửa sạch da và mắt với nước ngay lập tức.
Nguy cơ hít phải
Hít phải bụi Lanthan có thể gây ra các vấn đề về hô hấp, bao gồm viêm phổi và khí phế thũng.
Để đảm bảo an toàn khi sử dụng nguyên tố Lanthan, cần lưu ý những điểm sau:
- Mang trang thiết bị bảo hộ cá nhân: Khi sử dụng Lanthan, cần mang găng tay, kính bảo hộ, và khẩu trang để tránh tiếp xúc trực tiếp với da, mắt và đường hô hấp.
- Làm việc trong môi trường thông gió tốt: Cần làm việc với Lanthan trong môi trường thông gió tốt để tránh hít phải bụi Lanthan.
- Bảo quản Lanthan đúng cách: Lanthan cần được bảo quản trong hộp kín, tránh tiếp xúc với nước và không khí ẩm.
- Rửa tay sau khi sử dụng: Sau khi sử dụng Lanthan, cần rửa tay kỹ lưỡng với xà phòng và nước.
Trên đây là toàn bộ những kiến thức cơ bản về nguyên tố Lanthan mà chúng tôi đã tổng hợp. Hãy cùng đọc và khám phá thêm về chủ đề này!
Chúng tôi hy vọng rằng bài viết đã cung cấp cho bạn cái nhìn tổng quan và sâu sắc về nguyên tố Lanthan. Nếu bạn có bất kỳ câu hỏi hoặc muốn tìm hiểu thêm, đừng ngần ngại để lại comment dưới đây nhé!