Nguyên tố Dysprosi, với tên tiếng Anh là “Dysprosium” và kí hiệu hóa học là “Dy”, là một nguyên tố hóa học với số hiệu nguyên tử là 66. Là một phần của nhóm lantanit trong bảng tuần hoàn, Dysprosi nổi bật với các tính chất vật lý và hóa học đặc biệt, bao gồm khả năng hấp thụ nơtron và đặc tính từ tính xuất sắc. Trong bài viết này, yeuhoahoc.edu.vn sẽ cung bạn đọc tìm hiểu sâu hơn về định nghĩa, lịch sử hình thành, và vị trí của nguyên tố Dysprosi trong bảng tuần hoàn hóa học.
Giới thiệu về nguyên tố Dysprosi
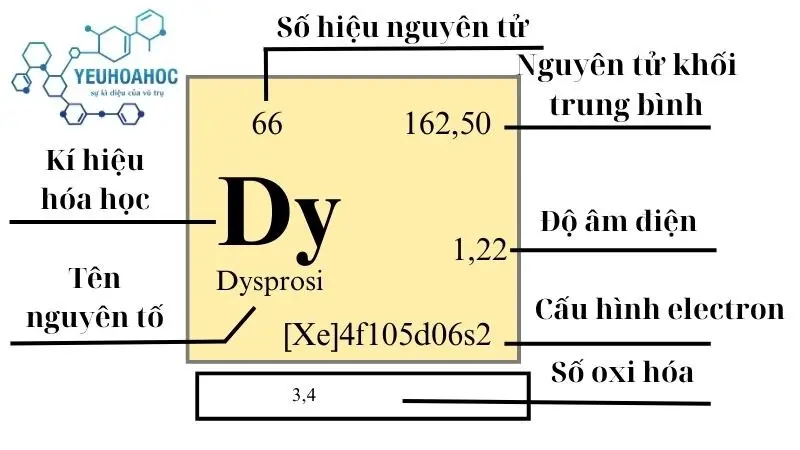
Định nghĩa
Nguyên tố Dysprosi là một nguyên tố kim loại đất hiếm với các tính chất từ tính mạnh mẽ, được sử dụng rộng rãi trong việc sản xuất các thiết bị từ và các ứng dụng công nghệ cao khác.
Lịch sử hình thành nguyên tố Dysprosi
1843: Carl Gustaf Mosander phát hiện ra terbia, một oxit của nguyên tố mới.
1879: Jean Charles Galissard de Marignac phân tích terbia và xác định nguyên tố mới, dysprosi.
1935: Wilhelm Klemm và Hans Bommer lần đầu tiên điều chế dysprosi kim loại.
Một số mốc thời gian quan trọng trong lịch sử phát hiện:
- 1843: Carl Gustaf Mosander phát hiện ra terbia.
- 1879: Jean Charles Galissard de Marignac xác định nguyên tố dysprosi.
- 1935: Wilhelm Klemm và Hans Bommer điều chế dysprosi kim loại.
- 1960: Dysprosi được sử dụng lần đầu tiên trong laser.
- 1970: Dysprosi được sử dụng trong các hợp kim để cải thiện độ bền và khả năng chống ăn mòn.
Nguyên tố Dysprosi trong bảng tuần hoàn hóa học
Trong bảng tuần hoàn, Dysprosi nằm trong nhóm lantanit, một phần của dãy nguyên tố đất hiếm.
- Thuộc nhóm: 3
- Chu kỳ: 6
- Khối lượng nguyên tử: 162,500 u
| Nhóm | Chu kỳ | Nguyên tử khối (u) | Khối lượng riêng g/cm3 | Nhiệt độ nóng chảy (K9) | Nhiệt độ bay hơi K | Nhiệt dung riêng J/g.K | Độ âm điện | Tỷ lệ trong vỏ Trái Đất mg/kg |
| 6 | 162,500 | 8,55 | 1680 | 2840 | 0,17 | 1,22 | 5,2 |
Tính chất của nguyên tố Dysprosi
Tính chất vật lý
- Dysprosi là kim loại đất hiếm, có màu trắng bạc, mềm, dẻo.
- Nó có cấu trúc tinh thể lục phương tâm kép ở nhiệt độ phòng.
- Dysprosi có nhiệt độ nóng chảy cao (1409 °C) và nhiệt độ sôi cao (2562 °C).
- Mật độ của Dysprosi là 8,54 g/cm³.
- Dysprosi có tính dẫn điện và dẫn nhiệt tốt.
- Dysprosi là kim loại thuận từ mạnh, nghĩa là nó bị hút vào từ trường.
Tính chất hóa học
- Dysprosi có hóa trị +3 trong hầu hết các hợp chất.
- Nó phản ứng với nước để tạo thành hydroxit dysprosi (Dy(OH)3).
- Dysprosi phản ứng với axit để tạo thành muối dysprosi.
- Dysprosi tác dụng với oxy để tạo thành dysprosi oxit (Dy2O3).
- Dysprosi có tính khử mạnh.
Ứng dụng của nguyên tố Dysprosi

Hợp kim
- Dysprosi được sử dụng để chế tạo hợp kim với các kim loại khác, ví dụ như hợp kim Nd-Fe-B dùng làm nam châm vĩnh cửu. Hợp kim này có khả năng chống khử từ cao, được sử dụng trong các tuabin gió và xe điện.
- Dysprosi cũng được sử dụng để chế tạo hợp kim với các kim loại khác như coban, vanadi, crom, v.v. để tạo ra các vật liệu có tính năng đặc biệt như độ bền cao, khả năng chống ăn mòn tốt, và tính dẫn nhiệt cao.
Laser
- Dysprosi được sử dụng để chế tạo laser Dy:YAG, được sử dụng trong nhiều ứng dụng khác nhau, bao gồm cắt, hàn, phẫu thuật, và tẩy lông. Laser Dy:YAG có bước sóng 2.36 μm, có khả năng hấp thụ tốt bởi các mô sinh học, do đó được sử dụng hiệu quả trong các ứng dụng y tế.
Y tế
- Dysprosi được sử dụng để điều trị một số bệnh, ví dụ như bệnh Gaucher. Dysprosi được sử dụng để làm thuốc tương phản trong chụp cộng hưởng từ (MRI).
- Dysprosi cũng được sử dụng để điều trị một số bệnh về mắt, ví dụ như thoái hóa điểm vàng.
Điện tử
- Dysprosi được sử dụng để chế tạo các linh kiện điện tử, ví dụ như tụ điện và bộ nhớ máy tính. Dysprosi có khả năng lưu trữ năng lượng từ cao, do đó được sử dụng để chế tạo các tụ điện có hiệu suất cao.
Năng lượng hạt nhân
- Dysprosi được sử dụng để điều khiển lò phản ứng hạt nhân. Dysprosi có khả năng hấp thụ neutron cao, do đó được sử dụng để chế tạo các thanh điều khiển lò phản ứng.
Điều chế và sản xuất nguyên tố Dysprosi
Điều chế
Điều chế trong phòng thí nghiệm
- Phương pháp khử ion kim loại:
- Điện phân dung dịch muối dysprosi(III) (như DyCl3) với điện cực catôt là kim loại thủy ngân.
- Phản ứng khử dysprosi(III) oxit (Dy2O3) bằng hydro hoặc kim loại kali.
Phương trình điều chế:
- Điện phân: DyCl3 + 3e- → Dy + 3Cl-
- Khử oxit: Dy2O3 + 3H2 → 2Dy + 3H2O
- Khử oxit: Dy2O3 + 6K → 2Dy + 3K2O
Điều chế trong công nghiệp
- Phương pháp chiết xuất dung môi:
- Chiết xuất dysprosi từ quặng monazit hoặc bastnäsit bằng dung môi hữu cơ.
- Lọc và tinh chế dung dịch dysprosi để thu được dysprosi tinh khiết.
Phương trình điều chế:
- Chiết xuất: DyCl3 + 3HA → DyA3 + 3HCl (HA là dung môi hữu cơ)
Sản xuất
- Dysprosi được sản xuất chủ yếu từ quặng monazit và bastnäsit.
- Quặng được nghiền nhỏ và xử lý bằng axit để hòa tan các kim loại đất hiếm.
- Dung dịch sau đó được chiết xuất bằng dung môi hữu cơ để thu được dysprosi.
- Dysprosi tinh khiết được thu được bằng cách lọc và tinh chế dung dịch.
Phản ứng của nguyên tố Dysprosi

Phản ứng với axit
Dysprosi phản ứng với axit để tạo thành muối dysprosi và khí hydro (H2).
Ví dụ:
- Dysprosi tác dụng với axit clohydric (HCl):
2Dy + 6HCl → 2DyCl3 + 3H2
- Dysprosi tác dụng với axit sulfuric (H2SO4):
Dy + 2H2SO4 → DySO4 + 2H2
Phản ứng với dung dịch muối
Dysprosi có thể phản ứng với dung dịch muối của một số kim loại khác để tạo thành kết tủa.
Ví dụ:
- Dysprosi tác dụng với dung dịch natri sunfat (Na2SO4):
DyCl3 + Na2SO4 → DySO4↓ + 2NaCl
- Dysprosi tác dụng với dung dịch kali cromat (K2CrO4):
DyCl3 + K2CrO4 → DyCrO4↓ + 2KCl
Phản ứng với oxy
Dysprosi tác dụng với oxy để tạo thành dysprosi oxit (Dy2O3).
Phương trình phản ứng:
4Dy + 3O2 → 2Dy2O3
Phản ứng với nước
Dysprosi phản ứng với nước để tạo thành dysprosi hydroxit (Dy(OH)3) và khí hydro (H2).
Phương trình phản ứng:
2Dy + 3H2O → 2Dy(OH)3 + H2
Lưu ý:
- Dysprosi là kim loại độc hại, cần cẩn thận khi sử dụng.
- Dysprosi phản ứng mãnh liệt với nước, nên bảo quản dysprosi trong môi trường khan.
Ngoài những phản ứng trên, Dysprosi còn có thể tham gia vào nhiều phản ứng hóa học khác.
Vấn đề an toàn khi sử dụng nguyên tố Dysprosi
Độc tính
- Dysprosi có thể gây ra độc tính nếu tiếp xúc với lượng lớn.
- Các triệu chứng ngộ độc dysprosi bao gồm buồn nôn, nôn, tiêu chảy, đau bụng, yếu cơ và co giật.
- Cần phải cẩn thận khi sử dụng dysprosi và tuân thủ các biện pháp an toàn để tránh ngộ độc.
Dị ứng
- Một số người có thể bị dị ứng với dysprosi.
- Các triệu chứng dị ứng dysprosi bao gồm phát ban, ngứa, sưng tấy và khó thở.
- Nếu bạn có bất kỳ triệu chứng dị ứng nào sau khi tiếp xúc với dysprosi, hãy ngừng sử dụng dysprosi và đến gặp bác sĩ ngay lập tức.
Nguy cơ môi trường
- Dysprosi có thể gây hại cho môi trường nếu thải ra môi trường không được kiểm soát.
- Cần phải xử lý chất thải dysprosi theo đúng quy định để bảo vệ môi trường.
Biện pháp an toàn
- Khi sử dụng dysprosi, cần phải tuân thủ các biện pháp an toàn sau:
- Mang găng tay, khẩu trang và kính bảo hộ khi tiếp xúc với dysprosi.
- Không được tiếp xúc trực tiếp với da và mắt.
- Làm việc trong khu vực thông gió tốt.
- Rửa tay kỹ sau khi tiếp xúc với dysprosi.
- Lưu trữ dysprosi trong một chiếc hộp đậy kín tại vị trí khô và mát.
Trên đây là toàn bộ những kiến thức cơ bản về nguyên tố Dysprosi mà chúng tôi đã tổng hợp. Hãy cùng đọc và khám phá thêm về chủ đề này!
Chúng tôi hy vọng rằng bài viết đã cung cấp cho bạn cái nhìn tổng quan và sâu sắc về nguyên tố Dysprosi. Nếu bạn có bất kỳ câu hỏi hoặc muốn tìm hiểu thêm, đừng ngần ngại để lại comment dưới đây nhé!