Khám phá xenlulozơ – thành phần chính của thành tế bào thực vật, mang vai trò quan trọng trong đời sống và tiềm năng ứng dụng rộng rãi trong nhiều lĩnh vực. Hãy cùng chúng tôi tìm hiểu về cấu tạo, nguồn gốc, vai trò và ứng dụng của xenlulozơ cùng các thông tin hữu ích khác trong bài viết này.
Khái niệm và đặc điểm cấu tạo của xenlulozơ
Định nghĩa
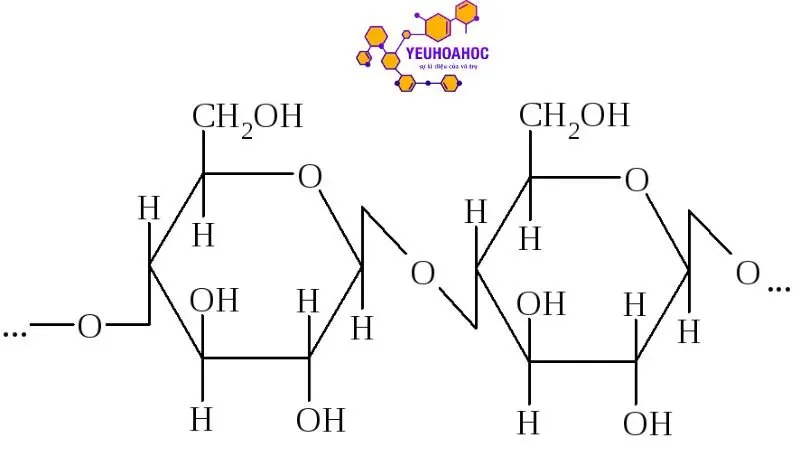
Xenlulozơ là một loại polisaccarit tự nhiên được tìm thấy nhiều nhất trong thành phần tế bào thực vật. Nó được cấu tạo từ các phân tử β-D-glucose liên kết với nhau bằng liên kết glycoside 1,4 β.
Đặc điểm cấu tạo
- Cấu trúc mạch không phân nhánh, hình sợi dài: Các phân tử β-D-glucose trong xenlulozơ được liên kết với nhau theo một chuỗi thẳng, không tạo thành nhánh. Điều này tạo nên cấu trúc dạng sợi dài, rắn chắc của xenlulozơ.
- Độ bền cơ học cao: Xenlulozơ có độ bền cơ học cao do sự liên kết chặt chẽ giữa các phân tử β-D-glucose trong chuỗi. Các liên kết glycoside 1,4 β tạo nên một mạng lưới liên kết hydro dày đặc, giúp tăng cường độ bền cho xenlulozơ.
- Khó tan trong nước: Xenlulozơ khó tan trong nước do cấu trúc dạng sợi không phân nhánh và các liên kết hydro giữa các phân tử. Nước không thể xâm nhập vào giữa các sợi xenlulozơ để tách chúng ra, dẫn đến việc xenlulozơ không tan trong nước.
- Có khả năng phản ứng với một số hóa chất: Xenlulozơ có thể phản ứng với một số hóa chất như axit, bazơ và một số enzyme. Các phản ứng này có thể thay đổi cấu trúc và tính chất của xenlulozơ.
Tính chất của xenlulozơ
Tính chất vật lý
Trạng thái: Rắn, dạng sợi
Màu sắc: Trắng
Độ tan:
Không tan trong nước
Tan trong dung dịch Cu(NH3)4(OH)2 (nước Svayde)
Tan trong một số dung môi hữu cơ như DMSO, DMF
Độ bền cơ học cao: Do cấu trúc mạch không phân nhánh và các liên kết hydro giữa các phân tử
Tính chất hóa học
Phản ứng thủy phân:
- Xenlulozơ có thể bị thủy phân thành glucozơ trong axit hoặc dưới tác dụng của enzyme xenlulaza.
Phản ứng cháy:
- Xenlulozơ cháy trong không khí tạo thành CO2, H2O và nhiệt.
Phản ứng với axit:
- Xenlulozơ có thể bị axit sunfuric cô đặc thủy phân thành cellodextrin.
Phản ứng với bazơ:
- Xenlulozơ có thể tan trong dung dịch Cu(NH3)4(OH)2 (nước Svayde) tạo dung dịch màu xanh lam.
So sánh tính chất của xenlulozơ với các loại polymer khác:
| Tính chất | Xenlulozơ | Tinh bột | PVC |
| Cấu trúc | Mạch không phân nhánh | Mạch phân nhánh | Mạch không phân nhánh |
| Độ bền cơ học | Cao | Trung bình | Cao |
| Độ tan | Khó tan trong nước | Tan trong nước nóng | Không tan trong nước |
| Khả năng phản ứng hóa học | Dễ phản ứng | Dễ phản ứng | Khó phản ứng |
| Ứng dụng | Sản xuất giấy, vải, tơ nhân tạo | Thực phẩm, sản xuất rượu bia | Ống nước, dây điện, vật liệu xây dựng |
Nguồn gốc và sự phân bố của xenlulozơ
Nguồn gốc chính
Xenlulozơ có nguồn gốc chính từ thành tế bào thực vật. Nó là thành phần chính của vách tế bào, giúp duy trì hình dạng và bảo vệ tế bào. Xenlulozơ được hình thành từ quá trình quang hợp, sử dụng năng lượng mặt trời để biến đổi CO2 và H2O thành glucose. Glucose sau đó được liên kết với nhau bằng liên kết glycosidic 1,4 β để tạo thành xenlulozơ.
Sự phân bố
Hàm lượng xenlulozơ trong các loại thực vật khác nhau có thể thay đổi tùy thuộc vào nhiều yếu tố như:
Loại thực vật:
- Cây thân gỗ thường có hàm lượng xenlulozơ cao hơn cây thân thảo.
- Một số loại cây có hàm lượng xenlulozơ cao đặc biệt như bông, gai, tre.
Bộ phận của cây:
- Vỏ cây thường có hàm lượng xenlulozơ cao hơn lõi cây.
- Lá cây thường có hàm lượng xenlulozơ cao hơn thân cây.
Độ tuổi của cây:
- Cây càng già thì hàm lượng xenlulozơ trong thành tế bào càng cao.
Điều kiện sinh trưởng:
- Điều kiện sinh trưởng thuận lợi như đủ ánh sáng, nước và dinh dưỡng có thể giúp cây tổng hợp xenlulozơ nhiều hơn.
Ví dụ về hàm lượng xenlulozơ trong một số loại thực vật phổ biến:
| Loại thực vật | Hàm lượng xenlulozơ (%) |
| Bông | 90-95 |
| Gai | 70-80 |
| Tre | 60-70 |
| Gỗ thông | 45-55 |
| Gạo | 30-35 |
| Khoai tây | 20-25 |
Cách điều chế xenlulozơ
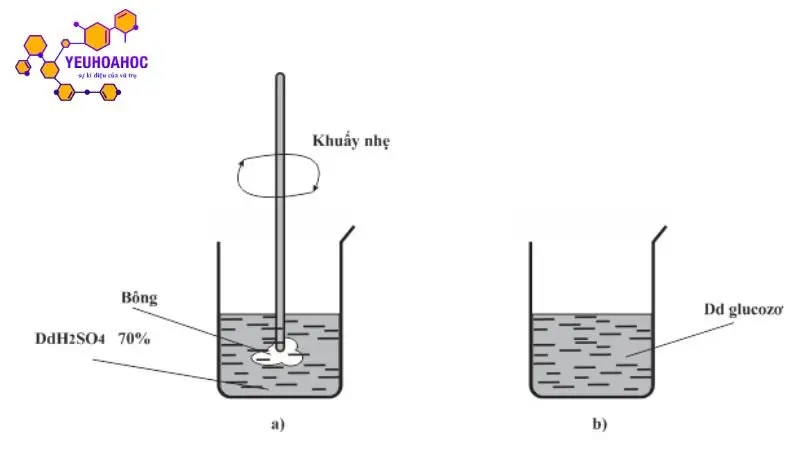
Trong phòng thí nghiệm
Có hai phương pháp chính để điều chế xenlulozơ trong phòng thí nghiệm:
Từ nguyên liệu thực vật:
Phương pháp chiết xuất:
Nghiền nhỏ nguyên liệu thực vật thành bột mịn.
Xử lý bột bằng dung dịch axit hoặc bazơ để loại bỏ các thành phần khác như protein, lignin, và pectin.
Rửa sạch bột bằng nước và làm khô.
Phương pháp thủy phân:
Thủy phân tinh bột hoặc cellulose acetate bằng axit hoặc enzyme để thu được xenlulozơ.
Từ dung dịch:
- Hòa tan xenlulozơ trong dung dịch Cu(NH3)4(OH)2 (nước Svayde).
- Lọc dung dịch và cho vào axit để kết tủa xenlulozơ.
- Rửa sạch xenlulozơ bằng nước và làm khô.
Trong công nghiệp
Trong công nghiệp, xenlulozơ được điều chế chủ yếu từ gỗ bằng phương pháp sulfit hoặc soda:
Phương pháp sulfit:
- Nghiền nhỏ gỗ thành bột mịn.
- Nấu bột gỗ với dung dịch SO2 và axit sunfuric ở nhiệt độ cao và áp suất cao.
- Rửa sạch bột giấy thu được và tẩy trắng bằng clo hoặc oxy già.
Phương pháp soda:
- Nghiền nhỏ gỗ thành bột mịn.
- Nấu bột gỗ với dung dịch NaOH ở nhiệt độ cao và áp suất cao.
- Rửa sạch bột giấy thu được và tẩy trắng bằng clo hoặc oxy già.
Ứng dụng của xenlulozơ
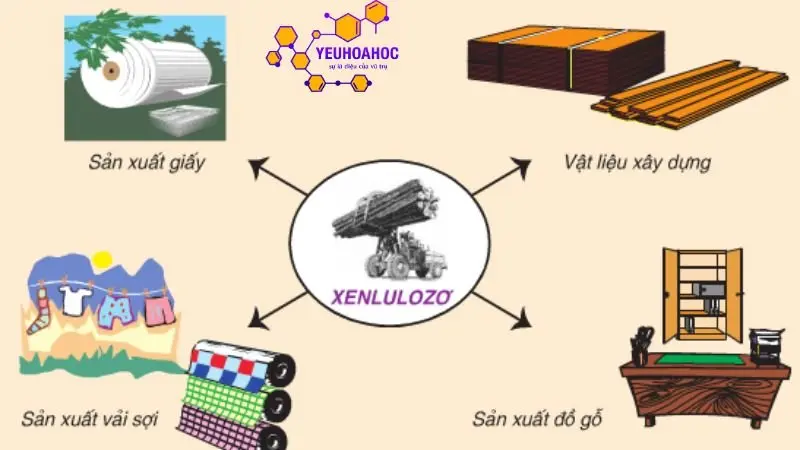
Ứng dụng trong công nghiệp
- Sản xuất giấy, bìa carton, bao bì: Xenlulozơ là nguyên liệu chính cho sản xuất giấy, bìa carton, bao bì. Giấy được làm từ các sợi xenlulozơ được liên kết với nhau bằng các liên kết hydro. Bìa carton được làm từ nhiều lớp giấy được ép lại với nhau. Bao bì được làm từ giấy hoặc bìa carton được phủ thêm các lớp nhựa hoặc kim loại để tăng độ bền và chống thấm nước.
- Sản xuất sợi, vải, quần áo: Xenlulozơ có thể được sử dụng để sản xuất các loại sợi như sợi visco, sợi rayon, sợi acetate. Các loại sợi này được sử dụng để dệt thành vải, quần áo và các sản phẩm dệt may khác.
- Sản xuất thuốc men, hóa chất: Xenlulozơ có thể được sử dụng để sản xuất các loại thuốc như thuốc giảm đau, thuốc hạ huyết áp, thuốc nhuận tràng. Xenlulozơ cũng được sử dụng để sản xuất các loại hóa chất như axeton, ethanol, axit axetic.
- Sản xuất các vật liệu xây dựng: Xenlulozơ có thể được sử dụng để sản xuất các loại vật liệu xây dựng như ván ép, tấm thạch cao, sơn. Ván ép được làm từ các lớp gỗ mỏng được dán lại với nhau bằng keo. Tấm thạch cao được làm từ lõi thạch cao được bọc bằng hai lớp giấy. Sơn được làm từ nhựa, bột màu và dung môi.
Ứng dụng trong đời sống
- Dùng trong thực phẩm: Xenlulozơ được sử dụng trong thực phẩm như chất tạo độ dày, chất ổn định, chất nhũ hóa. Xenlulozơ cũng được sử dụng để sản xuất các loại thực phẩm chức năng như chất xơ bổ sung.
- Dùng trong y tế: Xenlulozơ được sử dụng trong y tế như băng gạc, bông băng, chỉ khâu. Xenlulozơ cũng được sử dụng để sản xuất các loại thuốc như thuốc cầm máu, thuốc giảm đau.
- Dùng trong mỹ phẩm: Xenlulozơ được sử dụng trong mỹ phẩm như chất làm đẹp da, tóc. Xenlulozơ cũng được sử dụng để sản xuất các loại kem chống nắng, kem dưỡng ẩm.
Bài tập áp dụng
Bài tập 1: Phân tích mẫu xenlulozơ
Đề bài Một mẫu xenlulozơ nặng 5g được đốt cháy hoàn toàn. Khối lượng CO2 và H2O thu được lần lượt là 16.5g và 6.75g. Xác định thành phần phần trăm khối lượng của cacbon, hydro và oxy trong mẫu xenlulozơ.
Giải:
Bước 1: Tính số mol CO2 và H2O.
\[
n_{CO2} = \frac{16.5 \, \text{g}}{44 \, \text{g/mol}} = 0.375 \, \text{mol}
\]
\[
n_{H2O} = \frac{6.75 \, \text{g}}{18 \, \text{g/mol}} = 0.375 \, \text{mol}
\]
Bước 2: Tính lượng cacbon và hydro trong mẫu.
\[
m_C = 0.375 \, \text{mol} \times 12 \, \text{g/mol} = 4.5 \, \text{g}
\]
\[
m_H = 0.375 \, \text{mol} \times 2 \times 1 \, \text{g/mol} = 0.75 \, \text{g}
\]
Bước 3: Tính lượng oxy trong mẫu xenlulozơ.
\[
m_O = 5 \, \text{g} – (4.5 \, \text{g} + 0.75 \, \text{g}) = 0.25 \, \text{g}
\]
Bước 4: Tính phần trăm khối lượng của mỗi nguyên tố.
\[
\%C = \left(\frac{4.5 \, \text{g}}{5 \, \text{g}}\right) \times 100 = 90\%
\]
\[
\%H = \left(\frac{0.75 \, \text{g}}{5 \, \text{g}}\right) \times 100 = 15\%
\]
\[
\%O = \left(\frac{0.25 \, \text{g}}{5 \, \text{g}}\right) \times 100 = 5\%
\]
Bài tập 2: Tính năng lượng tỏa ra khi đốt cháy xenlulozơ
Đề bài: Tính năng lượng tỏa ra khi đốt cháy hoàn toàn 1 kg xenlulozơ, biết rằng năng lượng tỏa ra khi đốt cháy hoàn toàn 1 mol glucopyranose là -2808 kJ.
Giải:
Bước 1: Định lượng xenlulozơ.
Xenlulozơ là polymer của glucopyranose (C6H10O5)
Khối lượng mol của glucopyranose là 162 g/mol
Bước 2: Tính số mol glucopyranose trong 1 kg xenlulozơ.
\[n = \frac{1000 \, \text{g}}{162 \, \text{g/mol}} \approx 6.17 \, \text{mol}\]
Bước 3:Tính năng lượng tỏa ra.
\[\text{Năng lượng tỏa ra} = 6.17 \, \text{mol} \times 2808 \, \text{kJ/mol} = 17333.76 \, \text{kJ}\]
Xenlulozơ – một hợp chất hữu cơ đầy tiềm năng, hứa hẹn mang đến nhiều lợi ích cho con người. Sử dụng xenlulozơ một cách hợp lý và hiệu quả sẽ góp phần bảo vệ môi trường và thúc đẩy phát triển kinh tế – xã hội.







