Thủy ngân, một nguyên tố kỳ bí với bản chất lỏng ở nhiệt độ phòng, đã lôi cuốn và thách thức nhân loại từ thời cổ đại. Được biết đến với đặc tính độc đáo, Thủy ngân không chỉ có một vị trí quan trọng trong lịch sử khoa học mà còn trong nhiều lĩnh vực công nghiệp và y tế. Bài viết này yeuhoahoc.edu.vn sẽ cùng các bạn khám phá nguyên tố Thủy ngân từ định nghĩa, lịch sử phát hiện đến vai trò của nó trong bảng tuần hoàn hóa học.
Giới thiệu về nguyên tố Thủy Ngân
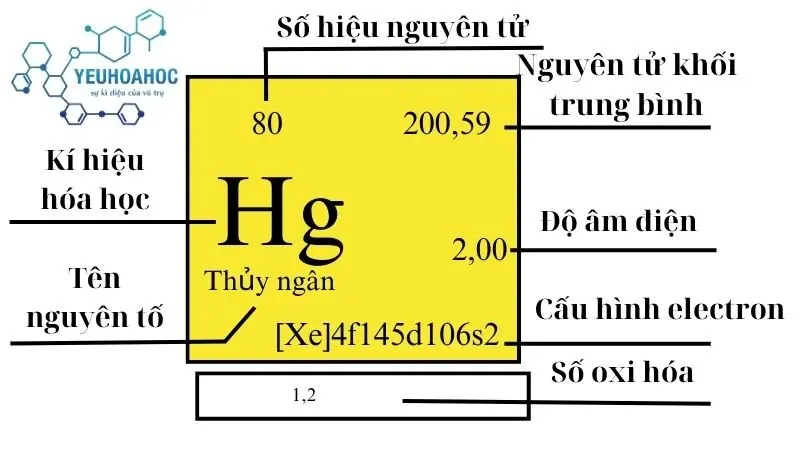
Định nghĩa
Thủy ngân, với tên tiếng Anh là “Mercury” và ký hiệu hóa học là “Hg” (phát xuất từ “Hydrargyrum” nghĩa là “bạc lỏng”), là nguyên tố hóa học có số nguyên tử là 80. Thủy ngân là một trong số ít các kim loại có tính lỏng ở nhiệt độ phòng, nổi bật với màu bạc sáng và khả năng dẫn điện tốt.
Lịch sử hình thành nguyên tố Thủy ngân
Lịch sử phát hiện:
- Thời cổ đại: Thủy ngân đã được biết đến từ thời cổ đại. Người Ai Cập, Hy Lạp, La Mã và Trung Quốc đã sử dụng nó trong các ứng dụng khác nhau.
- Thế kỷ 16: Paracelsus, một nhà giả kim thuật và thầy thuốc người Thụy Sĩ, đã sử dụng thủy ngân để điều trị bệnh giang mai.
- Thế kỷ 18: Thủy ngân được sử dụng trong nhiệt kế và áp kế.
- Thế kỷ 19: Thủy ngân được sử dụng trong các thiết bị điện, như bóng đèn huỳnh quang.
Một số mốc thời gian quan trọng
- 3000 TCN: Thủy ngân được sử dụng trong các lăng mộ Ai Cập.
- 1527: Paracelsus sử dụng thủy ngân để điều trị bệnh giang mai.
- 1714: Gabriel Fahrenheit phát minh ra nhiệt kế thủy ngân.
- 1879: Thomas Edison phát minh ra bóng đèn huỳnh quang.
- 1940: Thủy ngân được sử dụng trong các vũ khí hạt nhân.
- 1970: Tác hại của thủy ngân đối với sức khỏe con người và môi trường được nhận thức.
- 1990: Công ước Minamata về Thủy ngân được ký kết để giảm thiểu việc sử dụng và phát thải thủy ngân.
Nguyên tố Thủy ngân trong bảng tuần hoàn hóa học
Thủy ngân nằm ở ô số 80 trong bảng tuần hoàn hóa học, thuộc nhóm 12 (nhóm kẽm) và chu kỳ 6. Nó có cấu hình electron là [Xe] 4f14 5d10 6s2.
| Nhóm | Chu kỳ | Nguyên tử khối (u) | Khối lượng riêng g/cm3 | Nhiệt độ nóng chảy (K) | Nhiệt độ bay hơi K | Nhiệt dung riêng J/g.K | Độ âm điện | Tỷ lệ trong vỏ Trái Đất mg/kg |
| 12 | 6 | 200,592(3) | 13,5336 | 234,43 | 629,88 | 0,14 | 2 | 0,085 |
Tính chất của nguyên tố Thủy ngân (Hg)
Tính chất vật lý
- Trạng thái: Thủy ngân là kim loại lỏng ở điều kiện tiêu chuẩn (nhiệt độ và áp suất phòng).
- Màu sắc: Bạc trắng.
- Mật độ: 13,546 g/cm³, cao hơn nhiều so với các kim loại lỏng khác.
- Nhiệt độ nóng chảy: -38,83 °C.
- Nhiệt độ sôi: 356,73 °C.
- Dẫn điện: Dẫn điện tốt.
- Dẫn nhiệt: Dẫn nhiệt kém.
- Khối lượng riêng: 13,534 g/cm³.
- Độ căng bề mặt: Cao, tạo thành các giọt hình cầu hoàn hảo.
- Hơi thủy ngân: Độc hại và có thể gây ra các vấn đề sức khỏe nghiêm trọng.
Tính chất hóa học
- Tính khử: Yếu.
- Tính oxi hóa: Yếu.
- Khả năng phản ứng: Thủy ngân không phản ứng với hầu hết các axit và bazơ.
- Phản ứng với oxy: Phản ứng với oxy ở nhiệt độ cao để tạo thành oxit thủy ngân (II) (HgO).
- Phản ứng với lưu huỳnh: Phản ứng với lưu huỳnh để tạo thành hợp chất sulfide thủy ngân (HgS).
- Phản ứng với kim loại: Phản ứng với một số kim loại như vàng, bạc và đồng để tạo thành hợp kim.
- Hòa tan: Không tan trong nước, tan trong axit nitric.
Lưu ý:
- Thủy ngân là một kim loại độc hại và cần được xử lý cẩn thận.
- Hơi thủy ngân có thể gây ra các vấn đề sức khỏe nghiêm trọng, bao gồm tổn thương não, thận và phổi.
- Cần tuân thủ các biện pháp an toàn khi sử dụng và bảo quản thủy ngân.
Ứng dụng của nguyên tố Thủy ngân (Hg)
Trước đây
- Nhiệt kế: Thủy ngân được sử dụng trong nhiệt kế do tính dẫn nhiệt tốt, độ giãn nở đều và dễ đọc.
- Áp kế: Thủy ngân được sử dụng trong áp kế để đo áp suất do tính linh động và dễ đọc.
- Công tắc thủy ngân: Thủy ngân được sử dụng trong công tắc để điều khiển dòng điện do tính dẫn điện tốt và dễ dàng ngắt mạch.
- Pin: Thủy ngân được sử dụng trong pin do khả năng tạo ra dòng điện ổn định.
- Hợp kim: Thủy ngân được sử dụng để tạo hợp kim với các kim loại khác như vàng và bạc để cải thiện độ dẻo và tính dẫn điện.
- Y tế: Thủy ngân được sử dụng trong một số dụng cụ y tế như máy đo huyết áp và thuốc sát trùng do tính diệt khuẩn.
Hiện nay
- Do tính độc hại cao, việc sử dụng thủy ngân trong các ứng dụng trên đã bị hạn chế hoặc cấm hoàn toàn ở nhiều quốc gia.
- Các ứng dụng thay thế an toàn hơn cho thủy ngân đã được phát triển và sử dụng rộng rãi.
Điều chế và sản xuất nguyên tố Thủy ngân (Hg)
Điều chế
Điều chế trong phòng thí nghiệm
- Phương pháp nung nóng:
Phương pháp này nung nóng hợp chất của thủy ngân, ví dụ như HgO, HgS, Hg2Cl2, để thu được Hg.
Phương trình điều chế:
HgO → Hg + O2
HgS + Fe → Hg + FeS
Hg2Cl2 → Hg + HgCl2
Điều chế trong công nghiệp
- Phương pháp khai thác:
Thủy ngân được khai thác từ quặng cinnabar (HgS). Quặng cinnabar được nghiền nhỏ và nung nóng để thu được Hg.
Phương trình điều chế:
HgS → Hg + S
Sản xuất
- Việc sản xuất Hg ngày càng bị hạn chế do tính độc hại cao.
- Một số quốc gia đã cấm hoàn toàn việc sản xuất và sử dụng Hg.
- Các nhà sản xuất Hg cần tuân thủ các quy định an toàn nghiêm ngặt để bảo vệ môi trường và sức khỏe con người.
Một số ứng dụng hiện nay của thủy ngân:
- Khai thác vàng: Thủy ngân được sử dụng để tách vàng khỏi quặng.
- Nghiên cứu khoa học: Thủy ngân được sử dụng trong một số nghiên cứu khoa học, chẳng hạn như nghiên cứu về các phản ứng hóa học.
- Một số thiết bị chuyên dụng: Thủy ngân vẫn được sử dụng trong một số thiết bị chuyên dụng, chẳng hạn như đèn huỳnh quang.
Phản ứng của nguyên tố Thủy ngân (Hg)
Phản ứng với oxy
Thủy ngân phản ứng với oxy ở nhiệt độ cao để tạo thành oxit thủy ngân (II) (HgO).
Phương trình phản ứng:
Hg + O2 → HgO
Phản ứng với lưu huỳnh
Thủy ngân phản ứng với lưu huỳnh để tạo thành hợp chất sulfide thủy ngân (HgS).
Phương trình phản ứng:
Hg + S → HgS
Phản ứng với axit
Thủy ngân không phản ứng với hầu hết các axit, nhưng nó có thể phản ứng với axit nitric đặc để tạo thành muối nitrat thủy ngân (II) (Hg(NO3)2).
Phương trình phản ứng:
Hg + 4HNO3 → Hg(NO3)2 + 2NO2 + 2H2O
Phản ứng với kim loại
Thủy ngân có thể phản ứng với một số kim loại như natri, kali và canxi để tạo thành hợp kim.
Phương trình phản ứng:
2Hg + 2Na → Na2Hg2
Ví dụ cụ thể:
- Khi cho một viên kẽm vào dung dịch muối thủy ngân (II) nitrat (Hg(NO3)2), kẽm sẽ tan và thu được thủy ngân dạng lỏng.
Phương trình phản ứng:
Zn + Hg(NO3)2 → Zn(NO3)2 + Hg
- Khi nung nóng hỗn hợp bột lưu huỳnh và thủy ngân, hỗn hợp sẽ chuyển sang màu đen do tạo thành hợp chất sulfide thủy ngân (HgS).
Vấn đề an toàn của nguyên tố Thủy ngân
Tác hại của nguyên tố Thủy ngân

- Thủy ngân là một chất độc hại cho con người và môi trường.
- Tiếp xúc với thủy ngân có thể gây ra các vấn đề về sức khỏe như:
- Tổn thương hệ thần kinh
- Suy giảm trí nhớ
- Run rẩy
- Yếu cơ
- Mệt mỏi
- Khó thở
- Tổn thương thận
- Tổn thương gan
- Gây dị tật bẩm sinh
- Thủy ngân có thể tích tụ trong chuỗi thức ăn, gây nguy hại cho động vật hoang dã.
Nguy cơ phơi nhiễm Thủy ngân
- Hít phải hơi thủy ngân từ các thiết bị bị vỡ hoặc rò rỉ.
- Ăn phải cá bị ô nhiễm thủy ngân.
- Sử dụng các sản phẩm mỹ phẩm hoặc y tế có chứa thủy ngân.
- Phơi nhiễm với thủy ngân tại nơi làm việc..
Cách phòng tránh phơi nhiễm Thủy ngân
- Hạn chế sử dụng các sản phẩm chứa thủy ngân.
- Thay thế các thiết bị chứa thủy ngân bằng các thiết bị an toàn hơn.
- Cẩn thận khi sử dụng và xử lý thủy ngân.
- Rửa tay kỹ sau khi tiếp xúc với thủy ngân.
- Tránh tiêu thụ các loại cá chứa lượng thủy ngân cao.
- Sử dụng các biện pháp bảo hộ cá nhân khi tiếp xúc trực tiếp với thủy ngân trong môi trường làm việc.
Quy định về an toàn Thủy ngân
- Công ước Minamata về Thủy ngân là một hiệp ước quốc tế nhằm bảo vệ sức khỏe con người và môi trường khỏi tác hại của thủy ngân.
- Công ước Minamata cấm sản xuất, xuất khẩu và nhập khẩu một số sản phẩm chứa thủy ngân.
- Các quốc gia ký kết Công ước Minamata có nghĩa vụ thực hiện các biện pháp để giảm thiểu việc sử dụng và phát thải thủy ngân.
Dưới đây là bản tóm tắt các thông tin cơ bản về nguyên tố Thủy ngân mà chúng tôi đã thu thập. Mời bạn đọc tiếp và khám phá thêm thông tin về chủ đề này!
Chúng tôi mong rằng bạn đã có được một cái nhìn toàn diện và chi tiết về nguyên tố Thủy ngân qua bài viết này. Nếu có bất cứ thắc mắc nào hoặc bạn muốn tìm hiểu thêm, hãy thoải mái để lại lời bình luận ở phía dưới!