Khi nói đến các yếu tố quan trọng cho sức khỏe và công nghệ, không thể không nhắc đến nguyên tố Magnesi. Với một loạt các ứng dụng đa dạng và ý nghĩa trong cả y học và công nghiệp, Magnesi không chỉ là một nguyên tố hóa học thông thường mà còn là một phần không thể thiếu của cuộc sống hằng ngày của chúng ta. Bài viết này yeuhoahoc.edu.vn sẽ giới thiệu về nguyên tố Magnesi, bao gồm lịch sử, tính chất, ứng dụng, và các vấn đề an toàn liên quan.
Giới thiệu về nguyên tố Magnesi
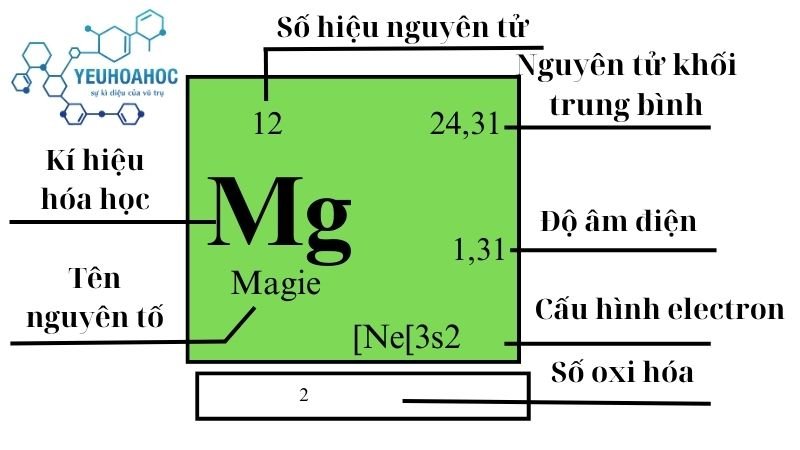
Magnesi là gì?
Magnesi có tên tiếng anh là Magnesium (ký hiệu: Mg, số nguyên tử: 12) là một nguyên tố hóa học thuộc nhóm kim loại kiềm thổ. Nó có màu trắng bạc, nhẹ, dễ dát mỏng và có tính khử mạnh. Magnesi là nguyên tố phổ biến thứ tám trong vỏ Trái đất và thứ tư trong vũ trụ.
Lịch sử phát hiện Magnesi
Magnesi được phát hiện vào năm 1755 bởi nhà khoa học người Anh Joseph Black. Ông đã nung nóng magnesia alba (magie cacbonat) và nhận thấy nó giải phóng một khí, sau này được xác định là khí cacbonic. Black đặt tên cho kim loại này là “magnesia”, theo tên vùng Magnesia ở Hy Lạp, nơi có nguồn magnesia alba dồi dào.
Mốc thời gian quan trọng:
- 1755: Joseph Black phát hiện ra Magnesi.
- 1808: Sir Humphry Davy lần đầu tiên điện phân Magnesi để thu được kim loại nguyên chất.
- 1831: Antoine Bussy điều chế Magnesi bằng phương pháp khử MgCl2 bằng kali.
- Cuối thế kỷ 19: Magnesi bắt đầu được sử dụng trong các hợp kim nhẹ cho ngành hàng không.
- Ngày nay: Magnesi được sử dụng rộng rãi trong nhiều lĩnh vực như công nghiệp, y tế, và nông nghiệp.
Tầm quan trọng của Magnesi
Magnesi đóng vai trò quan trọng trong tự nhiên và trong đời sống con người:
Trong tự nhiên:
- Magnesi là thành phần quan trọng của chlorophyll, sắc tố quang hợp của cây xanh.
- Magnesi là thành phần cấu tạo của nhiều khoáng chất, ví dụ như dolomit và magnesit.
- Magnesi là một trong những nguyên tố cấu tạo nên xương và răng của con người.
Trong đời sống con người:
- Magnesi là một cofactor cho hơn 300 enzyme trong cơ thể, tham gia vào nhiều quá trình quan trọng như:
- Chuyển hóa năng lượng
- Tổng hợp protein
- Chức năng thần kinh và cơ bắp
- Điều hòa huyết áp
- Sức khỏe tim mạch
Nguyên tố Magnesi trong bảng tuần hoàn các nguyên tố hóa học
Nguyên tố Magnesi (Mg) là một thành viên của bảng tuần hoàn hóa học, nằm ở hàng thứ hai và cột thứ hai bên trái của bảng. Với số nguyên tử là 12, nó thuộc về nhóm các kim loại kiềm thổ, cùng với các nguyên tố khác như Berili (Be), Canxi (Ca), Stronti (Sr), và Ba. Vị trí của Magnesi trong bảng tuần hoàn giúp xác định các tính chất hóa học và vật lý của nó, cũng như ảnh hưởng đến các ứng dụng trong nhiều lĩnh vực khác nhau.
| Nhóm | Chu kỳ | Nguyên tử khối (u) | Khối lượng riêng g/cm3 | Nhiệt độ nóng chảy (K9) | Nhiệt độ bay hơi
K |
Nhiệt dung riêng
J/g.K |
Độ âm điện | Tỷ lệ trong vỏ Trái Đất
mg/kg |
| 2 | 3 | 24,3059 | 1,738 | 923 | 1363 | 1,023 | 1,31 | 23300 |
Tính chất của nguyên tố Magnesi
Tính chất vật lý
- Magnesi là kim loại có màu trắng bạc, nhẹ, dễ dát mỏng.
- Khối lượng riêng của Magnesi là 1,738 g/cm³, nhẹ hơn nhôm.
- Nhiệt độ nóng chảy của Magnesi là 650°C, sôi ở 1090°C.
- Magnesi dẫn điện và dẫn nhiệt tốt.
- Magnesi có tính khử mạnh.
Tính chất hóa học
- Magnesi tác dụng với nước nóng để tạo thành magie hydroxit và khí hydro.
- Magnesi tác dụng với axit để tạo thành muối magie và khí hydro.
- Magnesi tác dụng với halogen để tạo thành muối magie halogenua.
- Magnesi cháy trong không khí với ngọn lửa màu trắng sáng.
Một số phản ứng hóa học của Magnesi
- Mg + 2H2O → Mg(OH)2 + H2
- Mg + 2HCl → MgCl2 + H2
- Mg + Br2 → MgBr2
- Mg + O2 → MgO
Ứng dụng của Magnesi

Hợp kim
- Magnesi được sử dụng để sản xuất hợp kim nhẹ, có độ bền cao.
- Hợp kim Magnesi được sử dụng trong ngành công nghiệp hàng không, ô tô, xe máy, và các thiết bị khác do tính nhẹ và bền.
- Một số ví dụ về hợp kim Magnesi bao gồm:
- Magnesi-nhôm: được sử dụng trong vỏ máy bay, vỏ xe ô tô, và các bộ phận xe máy.
- Magnesi-lithi: được sử dụng trong các thiết bị điện tử di động và các ứng dụng hàng không vũ trụ.
Hóa chất
- Magnesi được sử dụng để sản xuất các hợp chất Magnesi như MgO, MgCl2, MgSO4.
- Hợp chất Magnesi được sử dụng trong nhiều lĩnh vực như y học, nông nghiệp, công nghiệp:
- MgO được sử dụng trong sản xuất sứ, thủy tinh, và vật liệu chịu lửa.
- MgCl2 được sử dụng trong sản xuất muối tắm, thuốc nhuận tràng, và chất khử trùng.
- MgSO4 được sử dụng trong sản xuất phân bón, thuốc diệt nấm, và thuốc nhuận tràng.
Y học
- Magnesi được sử dụng để điều trị một số bệnh như loãng xương, chuột rút, và chứng đau nửa đầu.
- Magnesi là thành phần quan trọng của một số loại thuốc như thuốc chống co giật, thuốc hạ huyết áp, và thuốc an thần.
- Magnesi cũng có thể giúp cải thiện sức khỏe tim mạch, giảm nguy cơ mắc bệnh tiểu đường, và giảm nguy cơ đột quỵ.
Điều chế và sản xuất nguyên tố Magnesi
Điều chế
Magnesi được điều chế bằng phương pháp điện phân nóng chảy MgCl2.
Quy trình điều chế Magnesi bao gồm các bước sau:
Khai thác và tinh chế MgCl2:
-
- MgCl2 được khai thác từ nước biển, mỏ muối, hoặc hồ muối.
- MgCl2 được tinh chế bằng phương pháp kết tinh, lọc, và sấy khô
Điện phân MgCl2 nóng chảy:
-
-
- MgCl2 được nung nóng chảy ở nhiệt độ khoảng 700°C.
- Dòng điện được truyền qua dung dịch MgCl2 nóng chảy.
- Magnesi được giải phóng ở catôt dưới dạng kim loại lỏng.
- Clo được giải phóng ở anot dưới dạng khí
-
Thu gom Magnesi:
-
-
-
- Magnesi lỏng được thu gom trong khuôn hoặc được rót vào một bể chứa.
- Magnesi được làm nguội và đóng rắn.
-
-
Phương pháp điện phân MgCl2 nóng chảy có một số ưu điểm:
- Hiệu suất cao
- Sản phẩm có độ tinh khiết cao
- Dễ dàng vận hành
Tuy vậy, cách thức này cũng đi kèm với một số hạn chế:
- Tiêu hao năng lượng cao
- Chi phí đầu tư ban đầu cao
- Tạo ra khí thải độc hại (clo)
Ngoài phương pháp điện phân, Magnesi còn có thể được điều chế bằng phương pháp nhiệt luyện:
- Phương pháp Pidgeon: Magnesi được điều chế bằng cách khử MgO bằng ferrosilicon.
- Phương pháp silicothermic: Magnesi được điều chế bằng cách khử MgO bằng silicon.
Tuy nhiên, các phương pháp nhiệt luyện ít được sử dụng hơn phương pháp điện phân do hiệu suất thấp hơn và sản phẩm có độ tinh khiết thấp hơn.
Sản xuất Magnesi
- Magnesi được sản xuất trên quy mô lớn bằng phương pháp điện phân MgCl2 nóng chảy.
- Nhu cầu tiêu thụ Magnesi ngày càng tăng do ứng dụng rộng rãi trong các lĩnh vực như công nghiệp, y tế, và nông nghiệp.
Phản ứng của nguyên tố Magnesi

- Phản ứng với oxi:
Magnesi cháy trong oxi với ngọn lửa màu trắng sáng, tạo thành magie oxit (MgO).
2Mg + O2 → 2MgO
- Phản ứng với nước:
Magnesi tác dụng với nước nóng (không tác dụng với nước lạnh) để tạo thành magie hydroxit (Mg(OH)2) và khí hydro (H2).
Mg + 2H2O → Mg(OH)2 + H2
- Phản ứng với axit:
Magnesi tác dụng với axit để tạo thành muối magie và khí hydro.
Mg + 2HCl → MgCl2 + H2
- Phản ứng với halogen:
Magnesi tác dụng với halogen (như Cl2, Br2) để tạo thành muối magie halogenua.
Mg + Br2 → MgBr2
Ngoài ra, Magnesi còn có thể tham gia vào một số phản ứng hóa học khác như:
- Phản ứng với dung dịch muối kim loại:
Mg + CuSO4 → MgSO4 + Cu
- Phản ứng khử oxit kim loại:
Mg + Fe2O3 → MgO + 2Fe
Tồn tại và khai thác nguyên tố Magnesi
Magnesi là nguyên tố phổ biến thứ tám trong vỏ Trái đất, chiếm khoảng 2,3% khối lượng.
Magnesi tồn tại trong tự nhiên dưới dạng:
- Khoáng chất: Magnesit (MgCO3), dolomit (MgCa(CO3)2), brucit (Mg(OH)2), carnallit (KMgCl3·6H2O), v.v.
- Nước biển: Magnesi là nguyên tố phổ biến thứ ba trong nước biển, sau natri và clo.
- Sinh vật: Magnesi là thành phần quan trọng của chlorophyll, sắc tố quang hợp của cây xanh.
Khai thác Magnesi:
- Magnesi được khai thác từ các mỏ khoáng sản như magnesit và dolomit.
- Quá trình khai thác Magnesi bao gồm các bước sau:
- Khai thác quặng: Quặng được khai thác bằng phương pháp lộ thiên hoặc hầm lò.
- Sơ chế: Quặng được nghiền nhỏ và loại bỏ tạp chất.
- Beneficiation: Quặng được xử lý bằng các phương pháp như tuyển nổi, tuyển từ, v.v. để thu được MgO.
- Nung nóng: MgO được nung nóng ở nhiệt độ cao để tạo thành MgCl2.
- Điện phân: MgCl2 được điện phân để thu được Magnesi kim loại.
Vấn đề an toàn khi sử dụng nguyên tố Magnesi
Cháy nổ
- Magnesi có thể dễ dàng bắt lửa và cháy trong không khí, tạo ra ngọn lửa màu trắng sáng.
- Bột Magnesi có thể phát nổ nếu tiếp xúc với lửa hoặc tia lửa điện.
- Cần bảo quản Magnesi ở nơi khô ráo, tránh tiếp xúc với nhiệt độ cao và các chất oxy hóa mạnh.
Gây hại cho sức khỏe
- Hít phải bụi Magnesi có thể gây kích ứng hệ hô hấp.
- Tiếp xúc với Magnesi có thể gây kích ứng da và mắt.
- Nuốt phải Magnesi có thể gây ngộ độc.
- Cần sử dụng các biện pháp bảo hộ cá nhân như găng tay, khẩu trang, kính bảo hộ khi làm việc với Magnesi.
Tương tác với các chất khác
- Magnesi có thể phản ứng với các chất khác như axit, halogen, và nước để tạo ra các hợp chất nguy hiểm.
- Cần cẩn thận khi sử dụng Magnesi với các chất khác để tránh xảy ra phản ứng nguy hiểm.
Lưu ý:
- Cần tuân thủ các quy định an toàn khi sử dụng Magnesi.
- Tránh xa tầm tay trẻ em.
- Nếu xảy ra tai nạn, cần liên hệ ngay với cơ sở y tế gần nhất.
Dưới đây là một số biện pháp an toàn cụ thể khi sử dụng Magnesi
Bảo quản:
- Bảo quản Magnesi ở nơi khô ráo, thoáng mát, tránh tiếp xúc trực tiếp với ánh nắng mặt trời.
- Giữ Magnesi cách xa các nguồn nhiệt và các chất oxy hóa mạnh.
- Bảo quản Magnesi trong hộp kín hoặc thùng chứa phù hợp.
Sử dụng:
- Mang các biện pháp bảo hộ cá nhân như găng tay, khẩu trang, kính bảo hộ khi làm việc với Magnesi.
- Tránh để Magnesi tiếp xúc trực tiếp với da và mắt.
- Không hút thuốc hoặc ăn uống khi làm việc với Magnesi.
- Giữ cho khu vực làm việc sạch sẽ và thông thoáng.
Xử lý sự cố:
- Nếu Magnesi bị cháy, sử dụng bình chữa cháy loại B hoặc cát để dập lửa.
- Nếu Magnesi tiếp xúc với da, rửa sạch với xà phòng và nước.
- Nếu Magnesi tiếp xúc với mắt, rửa sạch với nước trong ít nhất 15 phút và đến gặp bác sĩ ngay lập tức.
- Nếu nuốt phải Magnesi, gọi ngay cho trung tâm chống độc hoặc đến gặp bác sĩ ngay lập tức.
Chất lượng và phương thức cung cấp nguyên tố Magnesi
Chất lượng Magnesi
Magnesi được cung cấp ở nhiều dạng khác nhau, bao gồm:
- Magnesi kim loại: dạng thỏi, dạng bột
- Hợp kim Magnesi
- Hợp chất Magnesi (như MgO, MgCl2, MgSO4)
Chất lượng Magnesi được đánh giá dựa trên các tiêu chí sau:
- Hàm lượng Magnesi
- Độ tinh khiết
- Kích thước hạt
- Hình dạng
Phương thức cung cấp Magnesi
Magnesi được cung cấp bởi các nhà sản xuất hóa chất và kim loại.
Magnesi có thể được mua trực tiếp từ các nhà sản xuất hoặc thông qua các nhà phân phối.
Phương thức cung cấp Magnesi phổ biến nhất là:
- Đóng gói trong bao bì kín
- Vận chuyển bằng container
- Lưu trữ trong kho
Dưới đây là tất cả những kiến thức cơ bản về nguyên tố Magnesi mà chúng tôi đã tổng hợp. Hãy cùng đọc và khám phá thêm về chủ đề này!
Chúng tôi hy vọng rằng bài viết đã cung cấp cho bạn cái nhìn tổng quan và sâu sắc về nguyên tố Magnesi. Nếu bạn có bất kỳ câu hỏi hoặc muốn tìm hiểu thêm, đừng ngần ngại để lại comment dưới đây nhé!









