Europi (Eu) là một trong những nguyên tố hiếm có trên Trái Đất, thuộc nhóm Lantanit của bảng tuần hoàn hóa học. Nguyên tố này nổi tiếng với ánh sáng phát quang mạnh mẽ, thường được sử dụng trong sản xuất màn hình TV, đèn LED, và nhiều ứng dụng quang học khác. Bài viết này yeuhoahoc.edu.vn sẽ cung cấp cái nhìn tổng quan về Europi, bao gồm định nghĩa, lịch sử, tính chất, ứng dụng, điều chế, và vấn đề an toàn liên quan.
Giới thiệu về nguyên tố Europi
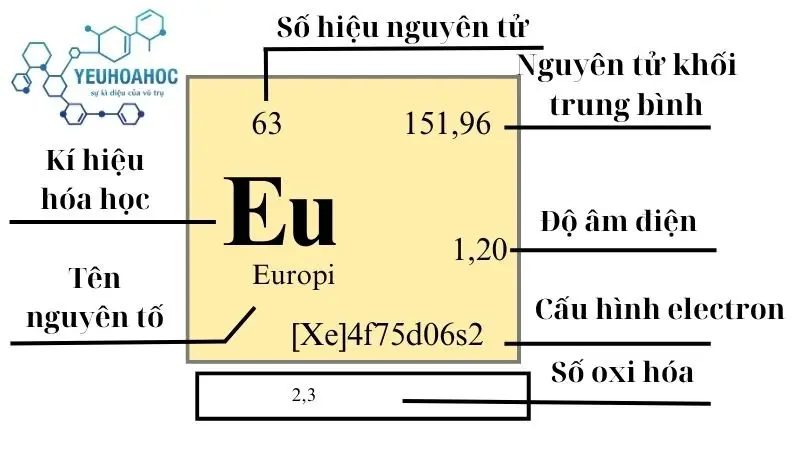
Định nghĩa
Europi, với tên tiếng Anh là “Europium” và kí hiệu hóa học là “Eu”, là một nguyên tố hóa học quan trọng thuộc nhóm Lantanit trong bảng tuần hoàn. Nổi bật với các tính chất đặc biệt và ứng dụng vô cùng rộng rãi, Europi chiếm một vị trí không thể thiếu trong nhiều lĩnh vực khoa học và công nghệ hiện đại.
Lịch sử hình thành nguyên tố Europi
1896: Paul Émile Lecoq de Boisbaudran phát hiện ra samari.
1901: Eugène Demarçay phân tích samari và phát hiện ra một nguyên tố mới, europi.
1960: Europi lần đầu tiên được sản xuất với số lượng lớn bằng cách khử ion europi trong dung dịch muối nóng chảy.
Một số mốc thời gian quan trọng trong lịch sử phát hiện:
- 1896: Paul Émile Lecoq de Boisbaudran phát hiện ra samari.
- 1901: Eugène Demarçay phân tích samari và phát hiện ra europi.
- 1925: George de Hevesy và Dirk Coster sử dụng phương pháp nhiễu xạ tia X để xác định cấu trúc tinh thể của europi.
- 1934: Wilhelm Klemm và Hans Bommer lần đầu tiên điều chế europi kim loại.
- 1960: Europi lần đầu tiên được sản xuất với số lượng lớn bằng cách khử ion europi trong dung dịch muối nóng chảy.
Nguyên tố Europi trong bảng tuần hoàn hóa học
- Thuộc nhóm: 3
- Chu kỳ: 6
- Khối lượng nguyên tử: 151,964(1) u
Trong bảng tuần hoàn, Europi được xếp vào nhóm nguyên tố Lantanit, nhóm này nổi tiếng với các nguyên tố có tính chất hóa học tương tự nhau. Europi là nguyên tố thứ 63, có số hiệu nguyên tử là 63.
| Nhóm | Chu kỳ | Nguyên tử khối (u) | Khối lượng riêng g/cm3 | Nhiệt độ nóng chảy (K9) | Nhiệt độ bay hơi K | Nhiệt dung riêng J/g.K | Độ âm điện | Tỷ lệ trong vỏ Trái Đất mg/kg |
| 6 | 151,964(1) | 5,243 | 1099 | 1802 | 0,182 | 1,2 | 2 |
Tính chất của nguyên tố Europi
Tính chất vật lý
- Trạng thái: Kim loại rắn, màu trắng bạc
- Khối lượng riêng: 5,264 g/cm³
- Điểm nóng chảy: 822 °C
- Điểm sôi: 1597 °C
- Độ cứng: Mohs 0,8
- Tính dẫn điện: Tốt
- Tính dẫn nhiệt: Tốt
Tính chất hóa học
- Trạng thái oxy hóa: +2, +3
- Tính khử: Mạnh
- Phản ứng với oxy: Dễ dàng phản ứng với oxy trong không khí tạo thành europi(III) oxit (Eu2O3)
- Phản ứng với nước: Tan trong nước tạo thành dung dịch hydroxit europi(II) (Eu(OH)2)
- Phản ứng với axit: Tan trong axit loãng tạo thành muối europi(II)
- Tính chất hóa học khác:
- Europi có tính khử mạnh hơn so với các kim loại đất hiếm khác.
- Europi có thể tạo thành các hợp chất với nhiều nguyên tố khác nhau, bao gồm hydro, oxy, halogen, nitơ, carbon và lưu huỳnh.
- Europi có thể phát quang màu đỏ khi được kích thích bởi bức xạ tia tử ngoại.
Ứng dụng của nguyên tố Europi

Lĩnh vực quang học
- Europi được sử dụng trong các loại đèn huỳnh quang để tạo ra ánh sáng đỏ.
- Europi được sử dụng trong các màn hình tivi CRT để tạo ra màu đỏ.
- Europi được sử dụng trong các laser để tạo ra ánh sáng có bước sóng hồng ngoại.
Lĩnh vực y học
- Europi-152 được sử dụng để chẩn đoán và điều trị ung thư.
- Europi-152 được sử dụng để chụp X-quang và MRI.
- Europi được sử dụng trong các loại thuốc để điều trị các bệnh về xương.
Lĩnh vực khoa học
- Europi được sử dụng trong các nghiên cứu khoa học về cấu trúc vật chất.
- Europi được sử dụng trong các nghiên cứu khoa học về tính chất vật liệu.
- Europi được sử dụng trong các nghiên cứu khoa học về môi trường.
Điều chế và sản xuất nguyên tố Europi

Điều chế nguyên tố Europi
Điều chế trong phòng thí nghiệm:
- Phương pháp khử ion Europi:
Phương pháp này sử dụng kim loại kiềm như kali hoặc natri để khử ion europi trong dung dịch muối nóng chảy. Ví dụ:
EuCl3 + 3K → Eu + 3KCl
Phương pháp điện phân:
Phương pháp này sử dụng dòng điện để khử ion europi trong dung dịch muối. Ví dụ:
EuCl3(aq) + 3e- → Eu(s) + 3Cl-(aq)
Điều chế trong công nghiệp:
- Phương pháp chiết xuất dung môi:
Phương pháp này sử dụng dung môi hữu cơ để chiết xuất europi từ quặng monazit. Europi sau đó được tách ra khỏi dung môi bằng cách kết tủa.
- Phương pháp trao đổi ion:
Phương pháp này sử dụng nhựa trao đổi ion để trao đổi ion europi với các ion khác trong dung dịch. Europi sau đó được tách ra khỏi nhựa bằng cách rửa bằng axit hoặc bazơ.
Sản xuất nguyên tố Europi
Europi được sản xuất chủ yếu bằng phương pháp chiết xuất dung môi. Quặng monazit được nghiền mịn và sau đó được xử lý bằng axit để hòa tan các kim loại đất hiếm. Dung dịch sau đó được chiết xuất bằng dung môi hữu cơ để chiết xuất europi. Europi sau đó được tách ra khỏi dung môi bằng cách kết tủa.
Lưu ý:
- Europi là một nguyên tố tương đối hiếm, vì vậy sản xuất europi khá tốn kém.
- Việc sản xuất europi có thể gây ra một số nguy cơ cho sức khỏe và môi trường, vì vậy cần phải có các biện pháp an toàn thích hợp.
Phản ứng của nguyên tố Europi
Phản ứng với oxy
Europi dễ dàng phản ứng với oxy trong không khí tạo thành europi(III) oxit (Eu2O3):
2Eu + 3O2 → Eu2O3
Phản ứng với nước
Europi tan trong nước tạo thành dung dịch hydroxit europi(II) (Eu(OH)2):
Eu + 2H2O → Eu(OH)2 + H2
Phản ứng với axit
Europi tan trong axit loãng tạo thành muối europi(II):
Eu + 2HCl → EuCl2 + H2
Phản ứng với halogen
Europi phản ứng với halogen (như Cl2, Br2, I2) tạo thành muối europi(III) halide:
2Eu + 3Cl2 → 2EuCl3
Phản ứng với kim loại khác
Europi có thể phản ứng với các kim loại khác (như Na, K) tạo thành hợp kim:
2Eu + 2Na → 2NaEu
Vấn đề an toàn khi sử dụng nguyên tố Europi
Nguy cơ cho sức khỏe
- Europi có thể gây kích ứng da, mắt và hệ hô hấp.
- Europi có thể gây hại cho gan, thận và hệ thần kinh.
- Europi có thể gây ung thư.
Nguy cơ cho môi trường
- Europi có thể gây ô nhiễm nước và đất.
- Europi có thể gây hại cho các sinh vật sống.
Biện pháp an toàn
- Khi sử dụng europi, cần phải đeo găng tay, khẩu trang và kính bảo hộ.
- Cần phải làm việc trong khu vực thông gió tốt.
- Cần phải xử lý europi theo đúng quy định.
Trên đây là toàn bộ những kiến thức cơ bản về nguyên tố Europi mà chúng tôi đã tổng hợp. Hãy cùng đọc và khám phá thêm về chủ đề này!
Chúng tôi hy vọng rằng bài viết đã cung cấp cho bạn cái nhìn tổng quan và sâu sắc về nguyên tố Europi. Nếu bạn có bất kỳ câu hỏi hoặc muốn tìm hiểu thêm, đừng ngần ngại để lại comment dưới đây nhé!