Cadmi, với tên tiếng Anh là “Cadmium” và kí hiệu hóa học là Cd, số nguyên tử 48, là một nguyên tố kim loại màu trắng ánh xanh, được biết đến với nhiều ứng dụng trong công nghiệp nhưng cũng đặt ra những lo ngại về môi trường và sức khỏe. Trong bài viết này, yeuhoahoc.edu.vn sẽ cùng các bạn khám phá nguyên tố Cadmi, từ định nghĩa cơ bản, quá trình phát hiện và lịch sử, đến vị trí và vai trò của nó trong bảng tuần hoàn hóa học, cũng như những lưu ý quan trọng về an toàn khi sử dụng.
Giới thiệu về nguyêh tô Cadmi
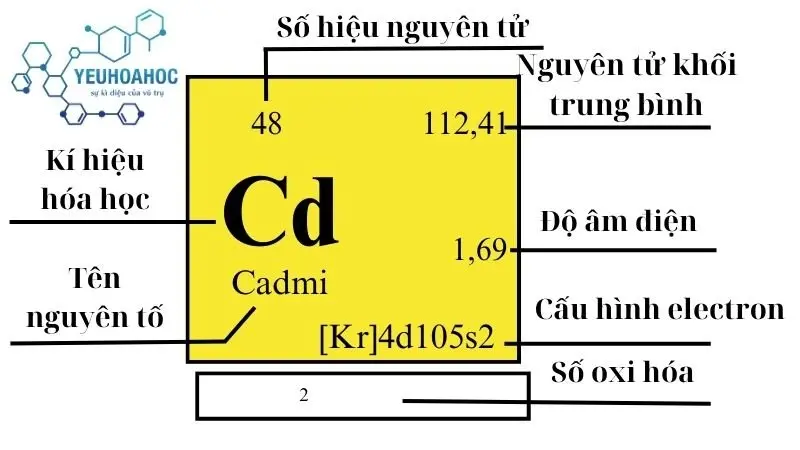
Định nghĩa
Cadmi tên tiếng anh là “Cadmium”, ký hiệu Cd – một nguyên tố hóa học mềm, dễ uốn, có màu trắng ánh xanh, thuộc nhóm 12 của bảng tuần hoàn hóa học. Cadmi thường được tìm thấy cùng với quặng kẽm và được sử dụng chủ yếu trong pin, hợp kim chống ăn mòn, và một số loại mực in.
Lịch sử hình thành nguyên tố Cadmi
1817: Friedrich Stromeyer và Carl Samuel Hermann, độc lập với nhau, phát hiện ra cadmi trong quặng kẽm. Stromeyer đặt tên cho nguyên tố mới này dựa trên từ “καδμία” (kadmeia), tên cổ đại của quặng kẽm, do sự xuất hiện của nó trong quặng này.
Mốc thời gian quan trọng:
- 1817: Friedrich Stromeyer, nhà hóa học người Đức, phát hiện ra Cadmi trong quặng kẽm.
- 1818: Stromeyer đặt tên cho nguyên tố này là Cadmi, theo tên tiếng Hy Lạp của quặng kẽm calamine.
- Thế kỷ 19: Cadmi bắt đầu được sử dụng trong mạ điện và hợp kim.
- Thế kỷ 20: Cadmi được sử dụng rộng rãi hơn trong các ứng dụng công nghiệp và y tế.
Nguyên tố Cadmi trong bảng tuần hoàn hóa học
Vị trí: Nhóm 12, chu kỳ 5
Cấu hình electron: [Kr] 4d¹⁰
Khối lượng nguyên tử: 112,411 u
| Nhóm | Chu kỳ | Nguyên tử khối (u) | Khối lượng riêng g/cm3 | Nhiệt độ nóng chảy (K9) | Nhiệt độ bay hơi K | Nhiệt dung riêng J/g.K | Độ âm điện | Tỷ lệ trong vỏ Trái Đất mg/kg |
| 12 | 5 | 112,411(8) | 8,69 | 594,22 | 1040 | 0,232 | 1,69 | 0,159 |
Tính chất của nguyên tố Cadmi
Tính chất vật lý
- Trạng thái: Rắn
- Màu sắc: Trắng ánh xanh
- Cấu trúc tinh thể: Lục giác
- Khối lượng riêng: 8,65 g/cm³
- Điểm nóng chảy: 321,07 °C
- Điểm sôi: 765 °C
- Độ dẫn điện: Cao
- Độ dẫn nhiệt: Cao
- Tính dẻo: Dẻo
- Tính dai: Dai
Tính chất hóa học
- Trạng thái oxy hóa: +2
- Tính khử: Yếu
- Tính oxi hóa: Mạnh
- Tác dụng với axit: Cadmi tan trong axit hydrochloric loãng và axit sulfuric loãng.
- Tác dụng với bazơ: Cadmi không tan trong bazơ.
- Tác dụng với kim loại: Cadmi tạo hợp kim với nhiều kim loại khác.
- Tác dụng với phi kim loại: Cadmi tạo hợp chất với nhiều phi kim loại khác.
Ứng dụng của nguyên tố Cadmi

Pin
Cadmi được sử dụng trong pin Ni-Cd để cung cấp năng lượng cho các thiết bị điện tử như máy tính xách tay và điện thoại di động. Tuy nhiên, do nguy cơ ô nhiễm môi trường và ảnh hưởng sức khỏe, pin Ni-Cd đang dần được thay thế bằng các loại pin khác an toàn hơn như pin lithium-ion.
Hợp kim
Cadmi được sử dụng để làm hợp kim với các kim loại khác như bạc và đồng để cải thiện độ bền và khả năng chống ăn mòn. Ví dụ, hợp kim Cadmi-bạc được sử dụng trong các thiết bị điện tử và hợp kim Cadmi-đồng được sử dụng trong các bộ phận của máy móc.
Mạ điện
Cadmi được sử dụng để mạ điện cho các kim loại khác như thép và kẽm để bảo vệ chúng khỏi bị ăn mòn. Tuy nhiên, do tính độc hại cao, việc sử dụng Cadmi để mạ điện đang được hạn chế và thay thế bằng các kim loại khác như kẽm và niken.
Ổn định nhựa
Cadmi được sử dụng để ổn định nhựa PVC để làm cho nó bền hơn và ít bị nứt hơn. Tuy nhiên, do nguy cơ ô nhiễm môi trường và ảnh hưởng sức khỏe, việc sử dụng Cadmi trong PVC đang dần được loại bỏ.
Ngoài ra, Cadmi còn có một số ứng dụng khác như:
- Sản xuất màu: Cadmi được sử dụng để sản xuất màu vàng và đỏ cho sơn và mực. Tuy nhiên, do nguy cơ ảnh hưởng sức khỏe, các loại màu thay thế an toàn hơn đang được sử dụng ngày càng phổ biến.
- Hàn: Cadmi được sử dụng trong các hợp kim hàn. Tuy nhiên, do tính độc hại, việc sử dụng Cadmi trong hàn đang được hạn chế.
- Ngành y tế: Cadmi được sử dụng trong một số loại thuốc. Tuy nhiên, do nguy cơ ảnh hưởng sức khỏe, việc sử dụng Cadmi trong y tế đang được hạn chế và thay thế bằng các loại thuốc khác an toàn hơn.
Điều chế và sản xuất nguyên tố Cadmi
Điều chế
Trong phòng thí nghiệm
- Cadmi có thể được điều chế bằng cách khử muối cadmi(II) bằng dung dịch kẽm hoặc kim loại kẽm. Ví dụ:
CdSO4 + Zn → Cd + ZnSO4
- Cadmi cũng có thể được điều chế bằng phương pháp điện phân dung dịch muối cadmi(II).
Trong công nghiệp
- Cadmi được sản xuất chủ yếu từ quặng kim loại như quặng kẽm, quặng chì và quặng đồng.
- Quặng kim loại được nghiền nát và nung chảy để chiết xuất các kim loại quý hiếm. Sau đó, Cadmi được tách ra khỏi các kim loại khác bằng phương pháp thủy luyện.
Phương trình điều chế
- Phương pháp khử:
CdSO4 + Zn → Cd + ZnSO4
- Phương pháp điện phân:
CdSO4 + H2O → Cd + O2 + 2H2SO4
Sản xuất
- Cadmi được sản xuất ở nhiều quốc gia trên thế giới, bao gồm Trung Quốc, Peru, Mexico và Hàn Quốc.
- Nhu cầu về Cadmi đang giảm dần do các nguy cơ về môi trường và sức khỏe liên quan đến việc sử dụng kim loại này.
Lưu ý:
- Cadmi là một kim loại nặng và có độc tính cao.
- Tiếp xúc với Cadmi có thể gây hại cho sức khỏe, bao gồm tổn thương thận, phổi và hệ thần kinh.
- Cần thực hiện các biện pháp phòng ngừa để đảm bảo an toàn khi sử dụng Cadmi.
Phản ứng hóa học của nguyên tố Cadmi

Phản ứng với axit
- Cadmi tan trong axit hydrochloric loãng và axit sulfuric loãng. Ví dụ:
Cd + 2HCl → CdCl2 + H2
Cd + 2H2SO4 → CdSO4 + 2H2
- Cadmi không tan trong axit nitric đặc.
Phản ứng với muối
- Cadmi có thể phản ứng với muối của các kim loại khác để tạo thành muối cadmi. Ví dụ:
Cd + 2AgNO3 → Cd(NO3)2 + 2Ag
Phản ứng oxy hóa khử
- Cadmi có thể thể hiện nhiều trạng thái oxy hóa khác nhau trong các phản ứng oxy hóa khử. Ví dụ:
Cd → Cd2+ + 2e-
Cd2+ + 2e- → Cd
Ví dụ cụ thể:
- Phản ứng của Cadmi với axit hydrochloric:
Cd + 2HCl → CdCl2 + H2
- Phản ứng của Cadmi với dung dịch muối bạc nitrat:
Cd + 2AgNO3 → Cd(NO3)2 + 2Ag
- Phản ứng oxy hóa khử của Cadmi:
Cd → Cd2+ + 2e-
Cd2+ + 2e- → Cd
Vấn đề an toàn khi sử dụng nguyên tố Cadmi
Cadmi là một kim loại nặng và có độc tính cao. Tiếp xúc với Cadmi có thể gây hại cho sức khỏe con người và môi trường.
Nguy cơ khi sử dụng Cadmi:
Đối với sức khỏe con người:
- Cadmi có thể gây tổn thương thận, phổi và hệ thần kinh.
- Cadmi có thể gây ung thư.
- Cadmi có thể ảnh hưởng đến hệ sinh sản và phát triển của thai nhi.
Đối với môi trường:
- Cadmi có thể tích tụ trong môi trường và gây ô nhiễm.
- Cadmi có thể gây hại cho các sinh vật sống trong môi trường.
Biện pháp phòng ngừa khi sử dụng Cadmi:
- Hạn chế tiếp xúc với Cadmi.
- Sử dụng các thiết bị bảo hộ cá nhân khi làm việc với Cadmi.
- Giữ cho khu vực làm việc thông gió tốt.
- Tuân thủ các quy định về an toàn lao động khi sử dụng Cadmi
Trên đây là toàn bộ những kiến thức cơ bản về nguyên tố Cadmi mà chúng tôi đã tổng hợp. Hãy cùng đọc và khám phá thêm về chủ đề này!
Chúng tôi hy vọng rằng bài viết đã cung cấp cho bạn cái nhìn tổng quan và sâu sắc về nguyên tố Cadmi. Nếu bạn có bất kỳ câu hỏi hoặc muốn tìm hiểu thêm, đừng ngần ngại để lại comment dưới đây nhé!