Bạc, với tên tiếng Anh là Silver và kí hiệu hóa học là Ag, là một trong những kim loại quý được biết đến và sử dụng rộng rãi từ thời cổ đại. Với số nguyên tử 47, bạc không chỉ nổi tiếng với vẻ đẹp màu trắng lấp lánh mà còn được đánh giá cao vì đặc tính dẫn điện và dẫn nhiệt tốt nhất trong tất cả các kim loại. Bài viết này yeuhoahoc.edu.vn sẽ cùng các bạn tìm hiểu nguyên tố bạc, từ định nghĩa cơ bản, lịch sử hình thành đến vị trí và vai trò của nó trong bảng tuần hoàn hóa học và ứng dụng trong cuộc sống.
Giới thiệu về nguyên tố Bạc
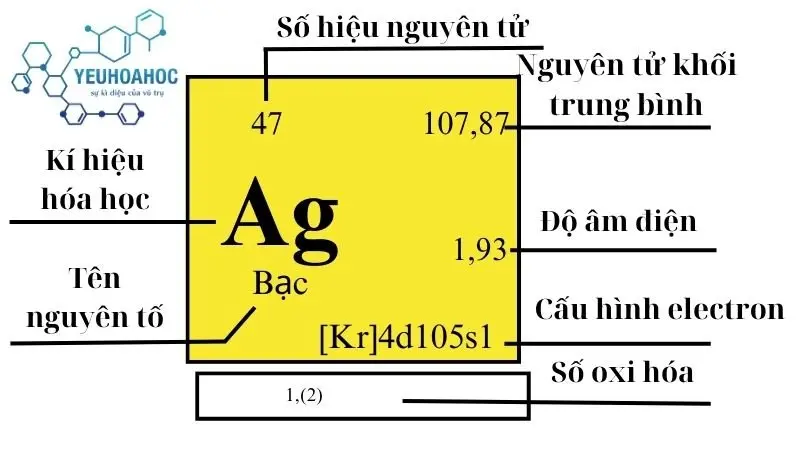
Định nghĩa
Bạc (Silver), với kí hiệu Ag từ từ Latin “Argentum”, là một nguyên tố hóa học thuộc nhóm kim loại chuyển tiếp. Kim loại này được biết đến với màu sắc trắng ánh kim đặc trưng, có độ bền cao, dễ dát mỏng và kéo dài.
Lịch sử hình thành nguyên tố Bạc
- Thời Cổ Đại: Bạc được sử dụng làm tiền tệ, trang sức, và đồ dùng gia đình ở nhiều nền văn minh cổ đại như Ai Cập, Hy Lạp, và La Mã.
- Thế Kỷ 12 – 18: Việc khám phá và khai thác mỏ bạc ở châu Âu và châu Mỹ đã góp phần vào sự thịnh vượng và mở rộng của các đế chế thời bấy giờ.
Một số mốc thời gian quan trọng trong lịch sử phát hiện:
- 3000 TCN: Bạc được sử dụng để làm đồ trang sức và đồ trang trí ở Ai Cập và Mesopotamia.
- 1200 TCN: Bạc được sử dụng làm tiền tệ ở Lydia.
- 1500 TCN: Bạc được sử dụng trong các ứng dụng y tế.
- 1800: Bạc được sử dụng trong nhiếp ảnh.
- 1900: Bạc được sử dụng trong điện tử.
Nguyên tố Bạc trong bảng tuần hoàn hóa học

Bạc nằm ở chu kỳ 5, nhóm 11 (IB) của bảng tuần hoàn hóa học. Nó là một kim loại chuyển tiếp mềm, dẻo và có khả năng dẫn điện và dẫn nhiệt cao. Bạc có một đồng vị bền là 107Ag.
| Nhóm | Chu kỳ | Nguyên tử khối (u) | Khối lượng riêng g/cm3 | Nhiệt độ nóng chảy (K9) | Nhiệt độ bay hơi K | Nhiệt dung riêng J/g.K | Độ âm điện | Tỷ lệ trong vỏ Trái Đất mg/kg |
| 11 | 5 | 107,8682(2) | 10,501 | 1234,93 | 2435 | 0,235 | 1,93 | 0,075 |
Tính chất của nguyên tố Bạc
Tính chất vật lý
- Trạng thái: Rắn
- Màu sắc: Trắng sáng
- Cấu trúc tinh thể: Lập phương tâm mặt
- Khối lượng riêng: 10,49 g/cm³
- Điểm nóng chảy: 961,8 °C
- Điểm sôi: 2212 °C
- Độ dẫn điện: Cao
- Độ dẫn nhiệt: Cao
- Tính dẻo: Dẻo
- Tính dai: Dai
Tính chất hóa học
- Trạng thái oxy hóa: +1
- Tính khử: Yếu
- Tính oxi hóa: Mạnh
- Tác dụng với axit: Bạc không tan trong hầu hết các axit.
- Tác dụng với bazơ: Bạc không tan trong bazơ.
- Tác dụng với kim loại: Bạc tạo hợp kim với nhiều kim loại khác.
- Tác dụng với phi kim loại: Bạc tạo hợp chất với nhiều phi kim loại khác.
Một số tính chất hóa học đặc biệt:
- Bạc có khả năng chống ăn mòn cao.
- Bạc có khả năng dẫn điện tốt.
- Bạc có khả năng diệt khuẩn.
Lưu ý:
- Bạc là một kim loại quý hiếm và đắt tiền.
- Bạc có thể gây hại cho sức khỏe nếu tiếp xúc với lượng lớn.
Ứng dụng của nguyên tố Bạc
Bạc là một kim loại quý hiếm có nhiều ứng dụng trong các lĩnh vực khác nhau
Trang sức và đồ trang trí
- Bạc được sử dụng rộng rãi để làm trang sức như vòng cổ, nhẫn, vòng tay và hoa tai.
- Bạc cũng được sử dụng để làm đồ trang trí như tượng, bình hoa và đồ dùng gia đình.
Tiền tệ
- Bạc được sử dụng để làm tiền xu và tiền giấy trong nhiều thế kỷ.
- Mặc dù ngày nay bạc không còn được sử dụng rộng rãi làm tiền tệ, nhưng nó vẫn được coi là một kim loại quý giá và được dự trữ bởi nhiều quốc gia.
Y tế
- Bạc có tính kháng khuẩn cao nên được sử dụng trong các dụng cụ y tế như kẹp, dao và nĩa.
- Bạc cũng được sử dụng để làm thuốc chống nấm và thuốc sát trùng.
Công nghiệp
- Bạc được sử dụng trong các thiết bị điện tử như pin, dây điện và bảng mạch.
- Bạc cũng được sử dụng trong các ứng dụng công nghiệp khác như hàn, nhiếp ảnh và sản xuất gương.
Các ứng dụng khác
- Bạc được sử dụng trong các sản phẩm lọc nước để diệt vi khuẩn.
- Bạc cũng được sử dụng trong các sản phẩm chăm sóc da để chống lão hóa và làm sáng da.
Điều chế và sản xuất nguyên tố Bạc
Điều chế
Trong phòng thí nghiệm
- Bạc có thể được điều chế bằng cách khử muối bạc(I) bằng dung dịch kẽm hoặc kim loại kẽm. Ví dụ:
AgNO3 + Zn → Ag + ZnNO3
- Bạc có thể tạo ra thông qua quá trình điện phân các dung dịch của muối bạc(I).
Trong công nghiệp
- Bạc được sản xuất chủ yếu từ quặng kim loại như quặng đồng, quặng chì và quặng kẽm.
- Quặng kim loại được nghiền nát và nung chảy để chiết xuất các kim loại quý hiếm. Sau đó, Bạc được tách ra khỏi các kim loại khác bằng phương pháp thủy luyện.
Phương trình điều chế:
- Phương pháp khử:
AgNO3 + Zn → Ag + ZnNO3
- Phương pháp điện phân:
AgNO3 + H2O → Ag + O2 + 2HNO3
Sản xuất
Bạc được sản xuất ở nhiều quốc gia trên thế giới, bao gồm Peru, Mexico, Trung Quốc và Nga.
Nhu cầu về Bạc đang tăng lên do các ứng dụng của nó trong các lĩnh vực như:
-
- Chế tạo đồ trang sức
- Chế tạo thiết bị điện tử
- Chế tạo pin
- Ngành y tế
Phản ứng hóa học của nguyên tố Bạc
Phản ứng với axit
- Bạc không tan trong axit hydrochloric loãng hoặc axit nitric loãng.
- Bạc tan trong axit sulfuric đặc nóng. Ví dụ:
Ag + 2H2SO4 → Ag2SO4 + 3H2
Phản ứng với muối halogen
- Bạc tan trong dung dịch muối halogen (như NaCl, KCl) tạo thành kết tủa bạc halogen (như AgCl, AgBr). Ví dụ:
Ag + Cl- → AgCl
Phản ứng với dung dịch kiềm
- Bạc không tan trong dung dịch kiềm.
Phản ứng oxy hóa khử
- Bạc có thể thể hiện nhiều trạng thái oxy hóa khác nhau trong các phản ứng oxy hóa khử. Ví dụ:
Ag + e- → Ag(0)
Ag + 2e- → Ag(-1)
Ví dụ cụ thể:
- Phản ứng của Bạc với axit sulfuric đặc nóng:
Ag + 2H2SO4 → Ag2SO4 + 3H2
- Phản ứng của Bạc với dung dịch natri clorua:
Ag + Cl- → AgCl
- Phản ứng oxy hóa khử của Bạc:
Ag + e- → Ag(0)
Ag + 2e- → Ag(-1)
Vấn đề an toàn khi sử dụng nguyên tố Bạc
Nguy cơ bụi Bạc

Bụi Bạc có thể gây kích ứng da, mắt và hệ hô hấp.
Hít phải bụi Bạc có thể dẫn đến các vấn đề về phổi như viêm phổi và xơ phổi.
Nguy cơ dị ứng
Có những cá nhân có thể phản ứng dị ứng với Bạc.
Các triệu chứng dị ứng Bạc có thể bao gồm phát ban, ngứa và sưng tấy.
Nguy cơ ngộ độc
Tiếp xúc với lượng lớn Bạc có thể dẫn đến ngộ độc.
Các triệu chứng ngộ độc Bạc có thể bao gồm buồn nôn, nôn mửa và tiêu chảy.
Để đảm bảo an toàn khi sử dụng Bạc, cần thực hiện các biện pháp phòng ngừa sau:
- Hạn chế tiếp xúc với bụi Bạc.
- Sử dụng các thiết bị bảo hộ cá nhân như găng tay, khẩu trang và kính bảo hộ khi làm việc với Bạc.
- Giữ cho khu vực làm việc thông gió tốt.
- Tuân thủ các quy định về an toàn lao động khi sử dụng Bạc.
Trên đây là toàn bộ những kiến thức cơ bản về nguyên tố Bạcmà chúng tôi đã tổng hợp. Hãy cùng đọc và khám phá thêm về chủ đề này!
Chúng tôi hy vọng rằng bài viết đã cung cấp cho bạn cái nhìn tổng quan và sâu sắc về nguyên tố Bạc. Nếu bạn có bất kỳ câu hỏi hoặc muốn tìm hiểu thêm, đừng ngần ngại để lại comment dưới đây nhé!