Khám phá bí ẩn của hạt nhân nguyên tử
Bài viết này sẽ đưa bạn đến gần hơn với thế giới vi mô qua việc tìm hiểu về hạt nhân nguyên tử, cấu tạo của nó và ký hiệu hạt nhân nguyên tử.
Hạt nhân nguyên tử, một khái niệm cơ bản nhưng vô cùng quan trọng trong lĩnh vực vật lý hạt nhân, là trung tâm của mọi nguyên tử và nắm giữ những bí mật sâu xa về cấu trúc vũ trụ. Bài viết này yeuhoahoc.edu.vn sẽ đưa bạn đến gần hơn với thế giới vi mô qua việc tìm hiểu về hạt nhân nguyên tử, cấu tạo của nó, công thức tính toán liên quan và ký hiệu hạt nhân nguyên tử.
Hạt Nhân Nguyên Tử Là Gì?

Hạt nhân nguyên tử là phần trung tâm của một nguyên tử, nơi chứa đựng hầu hết khối lượng của nguyên tử. Được cấu tạo từ hai loại hạt cơ bản là proton và neutron, hạt nhân mang một điện tích dương do số lượng proton quyết định.
Cấu Tạo Hạt Nhân Nguyên Tử
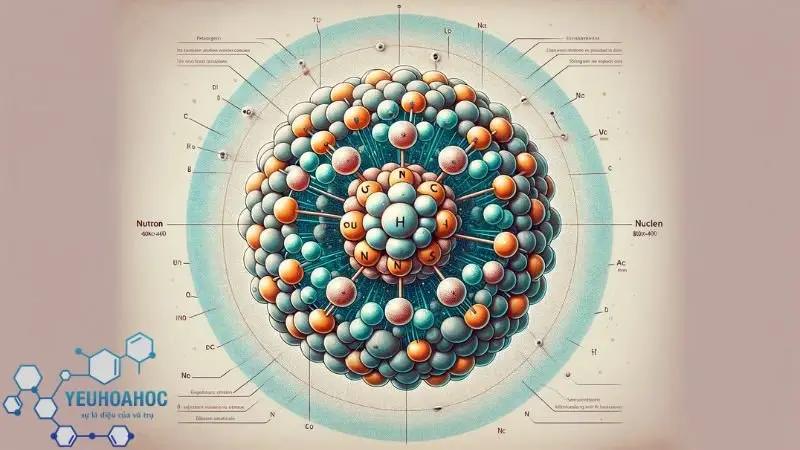
Hạt nhân nguyên tử được cấu tạo bởi hai loại hạt cơ bản là proton và neutron. Proton (p) điện tích dương, neutron (n) không mang điện tích.
- Proton: ký hiệu (p) Mang điện tích dương (+1), khối lượng khoảng
- Neutron: Ký hiệu (n) Không mang điện tích (0), khối lượng khoảng
.
Số proton có trong hạt nhân của một nguyên tố hóa học được gọi là số hiệu nguyên tử (Z). Số neutron có trong hạt nhân của một nguyên tố hóa học được gọi là số khối (A).
Ký hiệu nhân nguyên tử
Ký hiệu của hạt nhân nguyên tử thường được biểu thị như sau:
Trong biểu thức này:
- X đại diện cho ký hiệu hóa học của nguyên tố.
- Z, được gọi là số hạt proton hoặc số hiệu nguyên tử, đồng thời cũng là vị trí của nguyên tố trong bảng tuần hoàn các nguyên tố hóa học.
- A, hay số khối, chỉ tổng số hạt nuclon (proton và neutron) trong hạt nhân.
Từ đó, số neutron N trong hạt nhân có thể được tính bằng cách lấy số khối A trừ đi số hiệu nguyên tử Z. (N = A – Z)
Ví dụ nguyên tố Na:
( A = 23, Z = 11, N = A – Z = 11)
Kích cỡ hạt nhân
Hạt nhân của một nguyên tử là cực kỳ nhỏ, đến mức không thể quan sát trực tiếp bằng mắt thường. Thực tế, hạt nhân này nhỏ hơn so với toàn bộ nguyên tử khoảng 10,000 đến 100,000 lần.
Nếu xem hạt nhân nguyên tử như một quả cầu với bán kính R, chúng ta có thể thấy một mối liên hệ giữa R và số khối A thông qua một công thức cụ thể.
(m)
Các đồng vị
Đồng vị được hiểu là các hạt nhân cùng loại nguyên tố có số proton (Z) giống hệt nhau nhưng lại khác nhau về số neutron (N). Điều này dẫn đến sự khác biệt về số khối A giữa chúng, mặc dù chúng thuộc cùng một nguyên tố.
Lấy ví dụ
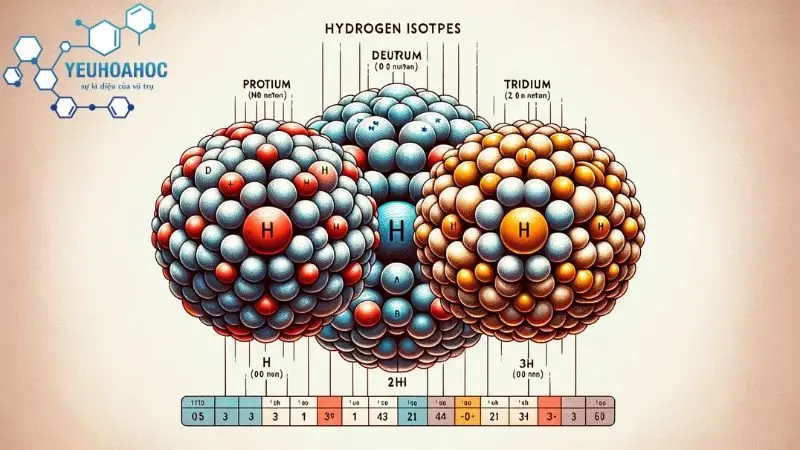
Nguyên tố Hydro có ba đồng vị phổ biến:
,
(được gọi là Dơtơri:
), và
(còn được biết đến là Triti:
).
Nguyên tử khối
Nguyên tử khối là khối lượng của một nguyên tử. Đơn vị của nguyên tử khối là đơn vị carbon (đvC) được quy ước là 1 đơn vị carbon thì bằng
khối lượng một nguyên tử carbon-12, ở trạng thái nghỉ.
Nguyên tử khối được tính bằng tổng khối lượng của các hạt cơ bản trong nguyên tử, bao gồm proton, neutron và electron. Tuy nhiên, khối lượng của electron rất nhỏ so với khối lượng của proton và neutron, nên khối lượng của nguyên tử gần bằng khối lượng của hạt nhân nguyên tử.
Hay nguyên tử khối chính là số khối (A)
Ví dụ: Nguyên tử khối của nguyên tố carbon là 12,011 (đvC).
Nguyên tố carbon có hai đồng vị là
và carbon
. Khối lượng của carbon
là 12,000 (đvC), còn khối lượng của carbon
là 13,003 (đvC).
Nguyên tử khối trung bình
Nguyên tử khối trung bình là khối lượng của một nguyên tử của một nguyên tố hóa học, được tính bằng cách tính trung bình cộng khối lượng của tất cả các đồng vị của nguyên tố đó.
Trong trường hợp một nguyên tố chỉ có một đồng vị, thì nguyên tử khối trung bình của nguyên tố đó bằng chính khối lượng của đồng vị đó.
Trong trường hợp một nguyên tố có nhiều đồng vị, thì nguyên tử khối trung bình của nguyên tố đó được tính theo công thức sau:
Trong đó:
- Avg là nguyên tử khối trung bình của nguyên tố
- w là phân bố tỉ lệ của các đồng vị trong tự nhiên
- A là nguyên tử khối của từng đồng vị
Ví dụ: Nguyên tố carbon có hai đồng vị là carbon
và carbon
. Phân bố tỉ lệ của carbon-12 trong tự nhiên là 98,89%, còn phân bố tỉ lệ của carbon-13 là 1,11%. Nguyên tử khối của carbon-12 là 12,000 (đvC), còn nguyên tử khối của carbon-13 là 13,003 (đvC).
Vậy nguyên tử khối trung bình của nguyên tố carbon là:
Avg = (0,9889 * 12,000 + 0,0111 * 13,003) / 1
Avg = 12,011 (đvC)
Như vậy, nguyên tử khối trung bình của nguyên tố carbon là 12,011 (đvC).
Công thức hạt nhân nguyên tử
Công thức hạt nhân nguyên tử thường liên quan đến số lượng proton (Z) và neutron (N) trong hạt nhân, với khối lượng hạt nhân được tính bằng công thức:
trong đó:
,
lần lượt là khối lượng của proton và neutron
: là năng lượng liên kết của hạt nhân
c là tốc độ ánh sáng trong chân không.
Điện tích hạt nhân nguyên tử là gì?
Điện tích hạt nhân nguyên tử là tổng điện tích của tất cả các proton trong hạt nhân nguyên tử. Mỗi proton mang một điện tích dương cố định, do đó, điện tích tổng cộng của hạt nhân được xác định bởi số lượng proton có trong đó. Vì mỗi proton mang điện tích là +1e (trong đó e là đơn vị điện tích cơ bản, khoảng 1.602×10-19 coulomb), điện tích của hạt nhân nguyên tử có thể được tính bằng cách nhân số lượng proton (được biểu thị bằng số hiệu nguyên tử, Z) với +1e Do đó, nếu một nguyên tử có Z proton, thì điện tích hạt nhân của nó sẽ là +Ze.
Điều này làm cho hạt nhân mang một điện tích dương rõ ràng, ảnh hưởng đến cách mà nguyên tử tương tác với các hạt khác và với bức xạ điện từ.
Bằng cách tận dụng sức mạnh của năng lượng trong hạt nhân, con người đã phát triển ra nhiều ứng dụng quan trọng trong ngành năng lượng hạt nhân, y học hạt nhân và nhiều lĩnh vực khác. Hiểu biết về cấu trúc và tính chất của hạt nhân nguyên tử không chỉ giúp chúng ta khám phá sâu hơn về bí ẩn của vũ trụ, mà còn mở ra cánh cửa cho nhiều phát minh và ứng dụng mới trong tương lai.







