Độ tan – một khái niệm tưởng chừng đơn giản nhưng lại ẩn chứa nhiều điều thú vị và ứng dụng quan trọng trong hóa học và thực tiễn. Bài viết này, yeuhoahoc.edu.vn sẽ đưa bạn đi sâu vào thế giới của độ tan, khám phá những bí ẩn về khả năng hòa tan của các chất trong nước. Hiểu rõ về độ tan sẽ giúp bạn giải quyết các vấn đề hóa học một cách hiệu quả, từ việc pha chế dung dịch đến tinh chế chất, xử lý nước thải,…
Định nghĩa và cách biểu thị độ tan
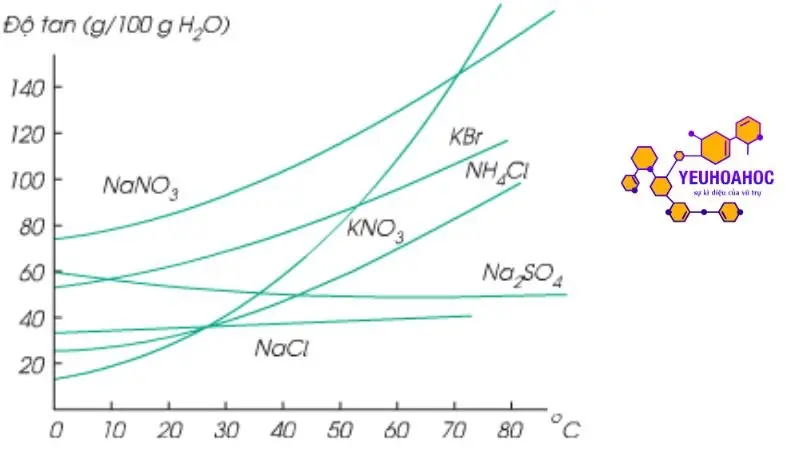
Độ tan là khái niệm biểu thị khả năng hòa tan của một chất trong một dung môi nhất định ở nhiệt độ và áp suất xác định. Nói cách khác, độ tan là số lượng tối đa của chất tan có thể hòa tan trong một lượng dung môi nhất định để tạo thành dung dịch bão hòa tại nhiệt độ và áp suất cụ thể.
Độ tan của một chất trong nước được định nghĩa là lượng gam của chất đó có thể được hòa tan trong 100 gam nước tạo thành dung dịch bão hòa tại một nhiệt độ nhất định.
Đơn vị thường dùng để biểu thị độ tan:
- Gam/lít (g/l): Đây là đơn vị phổ biến nhất, thể hiện số gam chất tan trong 1 lít dung dịch.
- Gam/100 gam dung môi (g/100g): Đơn vị này phù hợp khi cần so sánh độ tan của các chất trong cùng một dung môi.
- Mol/lít (mol/l): Đơn vị này thể hiện số mol chất tan trong 1 lít dung dịch, thường được sử dụng trong các tính toán hóa học.
Công thức tính độ tan theo khối lượng:
Công thức chung để tính độ tan theo khối lượng là:
Ví dụ:
- Ở 25°C, độ tan của NaCl trong nước là 36 g/100 g. Điều này có nghĩa là 100 g nước có thể hòa tan tối đa 36 g NaCl để tạo thành dung dịch bão hòa.
Công thức tính độ tan theo thể tích
Công thức chung để tính độ tan theo thể tích là:
Ví dụ:
- Ở 20°C, độ tan của KCl trong nước là 31,6 g/l. Điều này có nghĩa là 1 lít nước có thể hòa tan tối đa 31,6 g KCl để tạo thành dung dịch bão hòa.
Những yếu tố ảnh hưởng đến khả năng hòa tan của một chất trong nước.

Độ tan là đại lượng thể hiện khả năng hòa tan của một chất trong một dung môi nhất định ở điều kiện nhiệt độ và áp suất xác định. Độ tan của một chất bị ảnh hưởng bởi nhiều yếu tố, bao gồm:
Nhiệt độ
- Chất rắn: Hầu hết độ tan của chất rắn tăng theo nhiệt độ. Ví dụ, muối ăn (NaCl) có độ tan ở 20°C là 35,9 g/100g nước, nhưng ở 100°C độ tan của nó tăng lên đến 357 g/100g nước.
- Chất lỏng: Độ tan của chất lỏng trong nước ít phụ thuộc vào nhiệt độ. Ví dụ, độ tan của etanol (C2H5OH) trong nước ở 20°C là 8,33 g/100g nước và ở 100°C là 8,52 g/100g nước.
- Chất khí: Độ tan của chất khí trong nước giảm theo nhiệt độ. Ví dụ, độ tan của oxy (O2) trong nước ở 20°C là 8 mg/L, nhưng ở 100°C giảm xuống còn 2 mg/L.
Áp suất
Độ tan của chất khí trong nước tăng theo áp suất. Ví dụ, khi ta sục khí CO2 vào nước, dưới áp suất cao, ta có thể hòa tan được nhiều CO2 hơn so với điều kiện áp suất thường.
Tính chất của chất tan và dung môi
- Lực liên kết: Độ tan phụ thuộc vào lực liên kết giữa các phân tử chất tan và dung môi. Các chất có lực liên kết giữa các phân tử tương tự nhau (cực tính – cực tính, không cực tính – không cực tính) sẽ dễ tan trong nhau hơn. Ví dụ, nước (H2O) có lực liên kết hydro là cực tính, do đó nó tan dễ dàng trong các dung môi có lực liên kết hydro như etanol (C2H5OH) và axit axetic (CH3COOH).
- Cấu tạo: Các chất có cấu tạo phân tử gần giống nhau thường có độ tan tương tự nhau. Ví dụ, các ankan (paraffin) như CH4, C2H6, C3H8 đều tan ít trong nước.
Ví dụ về các trường hợp chất tan có cùng công thức hóa học nhưng độ tan khác nhau:
- NaCl: NaCl có độ tan trong nước ở 25°C là 35,9 g/100g nước, nhưng trong dung dịch axit clohidric (HCl) bão hòa, độ tan của nó có thể lên đến 58 g/100g nước.
- AgCl: AgCl có độ tan trong nước ở 25°C là 0,0018 g/100g nước, nhưng trong dung dịch amoniac (NH3) loãng, độ tan của nó có thể tăng lên đến 6,2 g/100g nước.
Kích thước hạt của chất rắn
Độ tan của chất rắn tăng theo kích thước hạt nhỏ. Lý do là vì khi kích thước hạt nhỏ, diện tích tiếp xúc giữa chất rắn và dung môi tăng, tạo điều kiện cho nhiều phân tử dung môi hòa tan được nhiều phân tử chất rắn hơn.
Phương pháp xác định độ tan của một chất tan trong nước
Có nhiều phương pháp khác nhau để xác định độ tan của một chất trong dung môi nhất định.
Phương pháp khuấy động
Nguyên tắc:
Phương pháp này dựa trên nguyên tắc cho chất tan vào dung môi và khuấy đều cho đến khi đạt được trạng thái bão hòa, tức là không thể hòa tan thêm chất tan vào dung dịch. Lúc này, lượng chất tan hòa tan trong dung dịch chính là độ tan của nó.
Cách thực hiện:
- Cân một lượng xác định chất tan vào một bình tam giác.
- Thêm dần dung môi vào bình tam giác và khuấy đều liên tục cho đến khi không còn cặn chất tan nào ở đáy bình.
- Ghi lại khối lượng dung môi đã sử dụng.
- Tính toán độ tan theo công thức:
Ưu điểm:
- Phương pháp đơn giản, dễ thực hiện.
- Không đòi hỏi thiết bị chuyên dụng.
- Có thể áp dụng cho nhiều loại chất tan khác nhau.
Nhược điểm:
- Độ chính xác có thể bị ảnh hưởng bởi kỹ thuật khuấy động.
- Khó xác định chính xác điểm bão hòa đối với một số chất tan.
Phương pháp đo độ bão hòa
Nguyên tắc:
Phương pháp này dựa trên nguyên tắc đo nồng độ của chất tan trong dung dịch bão hòa. Nồng độ này chính là độ tan của chất tan trong dung môi.
Cách thực hiện:
- Chuẩn bị một số dung dịch của chất tan có nồng độ khác nhau.
- Đo nồng độ của chất tan trong mỗi dung dịch bằng các phương pháp hóa học thích hợp (như phương pháp chuẩn độ, phương pháp quang phổ,…).
- Vẽ đồ thị biểu diễn mối quan hệ giữa nồng độ chất tan và độ tan.
- Xác định điểm bão hòa trên đồ thị, tại đó nồng độ chất tan đạt giá trị tối đa.
- Độ tan của chất tan chính là nồng độ chất tan tại điểm bão hòa.
Ưu điểm:
- Độ chính xác cao hơn phương pháp khuấy động.
- Có thể áp dụng cho nhiều loại chất tan khác nhau.
Nhược điểm:
- Cần có thiết bị và hóa chất chuyên dụng để đo nồng độ chất tan.
- Quy trình thực hiện phức tạp hơn so với phương pháp khuấy động.
Phương pháp sử dụng độ bão hòa bằng nhiệt
Nguyên tắc:
Phương pháp này dựa trên nguyên tắc làm lạnh hoặc làm nóng dung dịch bão hòa của chất tan cho đến khi bắt đầu kết tinh. Nhiệt độ lúc này chính là nhiệt độ bão hòa của chất tan. Từ nhiệt độ bão hòa, có thể tính toán độ tan của chất tan ở nhiệt độ đó bằng các bảng dữ liệu hoặc bằng các phương pháp tính toán hóa học.
Cách thực hiện:
- Chuẩn bị dung dịch bão hòa của chất tan.
- Làm lạnh hoặc làm nóng dung dịch bão hòa một cách chậm rãi và đều đặn.
- Ghi lại nhiệt độ tại thời điểm bắt đầu kết tinh.
- Tra cứu nhiệt độ bão hòa của chất tan ở nhiệt độ đã ghi lại trong bảng dữ liệu hoặc tính toán bằng các phương pháp hóa học.
- Độ tan của chất tan ở nhiệt độ đó chính là giá trị nhiệt độ bão hòa đã tra cứu hoặc tính toán.
Ưu điểm:
- Có thể xác định độ tan của chất tan ở nhiều nhiệt độ khác nhau.
- Phương pháp cho kết quả chính xác cao.
Nhược điểm:
- Cần có thiết bị chuyên dụng để làm lạnh hoặc làm nóng dung dịch.
- Quy trình thực hiện phức tạp hơn so với hai phương pháp trước.
Lựa chọn phương pháp phù hợp:
Việc lựa chọn phương pháp xác định độ tan phù hợp phụ thuộc vào nhiều yếu tố, bao gồm:
- Loại chất tan cần xác định độ tan.
- Độ chính xác mong muốn.
- Thiết bị và hóa chất sẵn có.
Ứng dụng của độ tan của một chất tan trong nước
Trong đời sống
- Pha chế dung dịch muối, đường,… để sử dụng trong nấu ăn, bảo quản thực phẩm: Độ tan của muối và đường trong nước giúp chúng ta pha chế dung dịch có nồng độ phù hợp cho các mục đích sử dụng khác nhau. Ví dụ, dung dịch muối được sử dụng để bảo quản thực phẩm, làm gia vị trong nấu ăn, dung dịch đường được sử dụng để pha chế nước giải khát, làm bánh kẹo,…
- Làm đá lạnh, kem,…: Nước có độ tan cao đối với CO2 ở nhiệt độ thấp. Khi hạ nhiệt độ, CO2 hòa tan trong nước sẽ bay ra ngoài, làm cho nước đông lạnh và tạo thành đá lạnh. Quá trình này cũng được áp dụng trong sản xuất kem, giúp tạo ra kết cấu kem mịn và xốp.
- Tinh chế các chất rắn: Độ tan khác nhau của các chất trong cùng một dung môi được sử dụng để tinh chế các chất rắn. Ví dụ, trong quá trình sản xuất muối ăn, nước được sử dụng để hòa tan muối thô, sau đó lọc bỏ cặn tạp chất và cô đặc dung dịch để thu được muối tinh thể.
Trong sản xuất
- Ngành công nghiệp thực phẩm: Độ tan được ứng dụng trong nhiều quy trình sản xuất thực phẩm, bao gồm: sản xuất nước giải khát, bia, rượu, nước mắm, tương,…
- Ngành khai thác khoáng sản: Độ tan của các khoáng sản trong nước được sử dụng để tách chiết và thu hồi kim loại. Ví dụ, quặng đồng được nghiền nhỏ và hòa tan trong dung dịch axit sunfuric, sau đó sử dụng phương pháp điện phân để thu hồi đồng kim loại.
- Ngành xử lý nước thải: Độ tan của các chất ô nhiễm trong nước được sử dụng để đánh giá hiệu quả của các phương pháp xử lý nước thải. Ví dụ, độ tan của BOD (nhu cầu oxy sinh học) trong nước là chỉ tiêu quan trọng để đánh giá mức độ ô nhiễm của nước thải.
Bài tập vận dụng
Bài 1: Tính độ tan của NaCl trong nước ở 25°C
Đề bài: Độ tan của NaCl trong nước ở 25°C là 36 g NaCl/100 g nước. Hỏi có thể hòa tan bao nhiêu gam NaCl vào 200 g nước ở nhiệt độ này để tạo thành dung dịch bão hòa?
Lời giải:
- Độ tan của NaCl là 36 g NaCl/100 g nước, nghĩa là trong 100 g nước có thể hòa tan tối đa 36 g NaCl.
- Để tính lượng NaCl có thể hòa tan trong 200 g nước, ta áp dụng tỉ lệ thẳng:
- Vậy, có thể hòa tan 72 g NaCl vào 200 g nước để tạo thành dung dịch bão hòa.
Bài 2: Ảnh hưởng của nhiệt độ đến độ tan của KNO3
Đề bài: Độ tan của KNO3 ở 20°C là 32 g KNO3/100 g nước và ở 60°C là 110 g KNO3/100 g nước. Hãy tính xem khi làm lạnh 500 g dung dịch bão hòa KNO3 từ 60°C xuống 20°C thì có bao nhiêu gam KNO3 tách ra khỏi dung dịch?
Lời giải:
Ở 60°C, độ tan của KNO3 là 110 g/100 g nước. Vậy trong 500 g nước có thể hòa tan:
Ở 20°C, độ tan của KNO3 là 32 g/100 g nước. Vậy trong 500 g nước có thể hòa tan:
Lượng KNO3 tách ra khi làm lạnh từ 60°C xuống 20°C là:
- Vậy, 390 g KNO3 sẽ tách ra khỏi dung dịch khi làm lạnh dung dịch từ 60°C xuống 20°C.
Những bài tập này giúp bạn hiểu rõ cách tính độ tan và những yếu tố ảnh hưởng đến độ tan của một chất trong dung môi, cụ thể là nước.
Độ tan – một kiến thức nền tảng thiết yếu trong hóa học, đóng vai trò quan trọng trong nhiều lĩnh vực đời sống và sản xuất. Hiểu biết về độ tan sẽ giúp bạn giải quyết các vấn đề hóa học một cách khoa học, hiệu quả, góp phần nâng cao chất lượng cuộc sống và bảo vệ môi trường. Hãy khám phá thêm về thế giới thú vị của độ tan để mở rộng kiến thức và ứng dụng nó vào thực tiễn một cách hiệu quả nhất!







