Bảng tuần hoàn hóa học, một trong những công cụ quan trọng nhất trong ngành hóa học, là chìa khóa mở cánh cửa hiểu biết về thế giới nguyên tử và các nguyên tố hóa học. Được Dmitri Mendeleev phát triển vào năm 1869, bảng tuần hoàn không chỉ là bảng liệt kê các nguyên tố mà còn là một hệ thống phân loại dựa trên tính chất đặc trưng, giúp các nhà khoa học dễ dàng nắm bắt và dự đoán được tính chất của các nguyên tố. Hãy cùng yeuhoahoc.edu.vn khám phá những điều cơ bản nhất và mẹo học bảng toàn hoàn hoá học dễ thuộc nhất qua bài viết dưới đây
Bảng tuần hoàn hoá học là gì?
Bảng tuần hoàn hóa học là sự sắp xếp có hệ thống của tất cả các nguyên tố hóa học dựa trên số hiệu nguyên tử, cấu hình electron và tính chất hóa học. Bảng này chia các nguyên tố thành các hàng (chu kỳ) và cột (nhóm) dựa trên các đặc điểm chung, giúp tiên đoán được tính chất và phản ứng của chúng.
Cấu tạo bảng tuần hoàn hoá học
Cấu tạo của Bảng Tuần Hoàn Hóa Học được thiết kế một cách khoa học để phản ánh mối quan hệ giữa các nguyên tố cũng như để tiên đoán được tính chất của chúng dựa trên vị trí trong bảng. Dưới đây là các thành phần chính của cấu tạo bảng tuần hoàn:
Ô nguyên tố
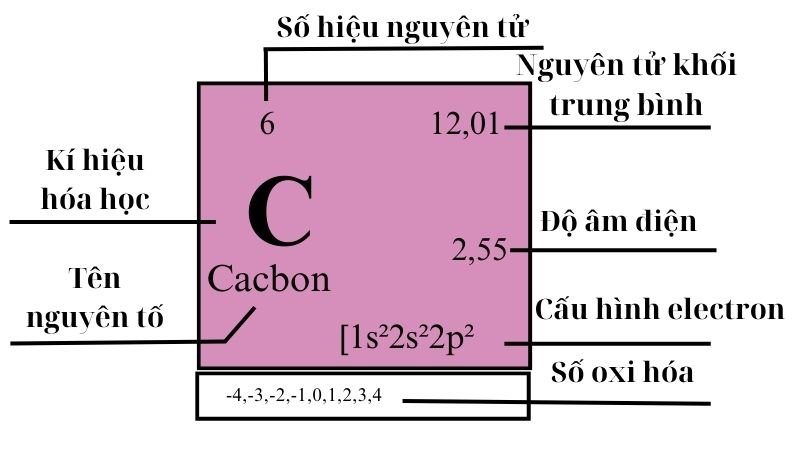
- Mỗi ô trong bảng tuần hoàn đại diện cho một nguyên tố hóa học duy nhất.
- Trong mỗi ô, thông tin cơ bản về nguyên tố được hiển thị, bao gồm ký hiệu hóa học, số hiệu nguyên tử, và khối lượng nguyên tử trung bình.
- Một số ô cũng có thể chứa thông tin bổ sung như trạng thái vật chất ở điều kiện tiêu chuẩn (rắn, lỏng, khí) và màu sắc của nguyên tố.
Chu kỳ
- Các chu kỳ trong bảng tuần hoàn được biểu thị bằng các hàng ngang, từ chu kỳ 1 đến chu kỳ 7.
- Mỗi chu kỳ tương ứng với việc thêm một lớp electron mới vào cấu hình electron của nguyên tử, bắt đầu từ lớp gần nhân nhất.
- Các nguyên tố trong cùng một chu kỳ có số lớp electron bằng nhau nhưng tính chất hóa học có thể thay đổi đáng kể từ trái sang phải.
- Các nhóm trong bảng tuần hoàn được biểu thị bằng các cột dọc, từ nhóm 1 đến nhóm 18.
- Các nguyên tố trong cùng một nhóm có số electron lớp ngoài cùng giống nhau, dẫn đến những tính chất hóa học tương tự nhau.
- Có những nhóm đặc biệt như nhóm kim loại kiềm (nhóm 1), kim loại kiềm thổ (nhóm 2), halogen (nhóm 1, 7), và khí hiếm (nhóm 1, 8) được biết đến với những tính chất đặc trưng.
Ý nghĩa của bảng tuần hoàn
Bảng tuần hoàn hóa học mang một ý nghĩa sâu sắc và đa dạng trong lĩnh vực khoa học, đặc biệt là trong ngành hóa học và vật lý. Dưới đây là một số ý nghĩa chính của bảng tuần hoàn:
Phân loại nguyên tố:
Bảng tuần hoàn cung cấp một cách hệ thống để phân loại tất cả các nguyên tố hóa học dựa trên số hiệu nguyên tử, từ đó giúp nhận diện và tổ chức thông tin về các nguyên tố một cách rõ ràng và có hệ thống.
Tiên đoán tính chất hóa học
Dựa vào vị trí của nguyên tố trong bảng tuần hoàn, có thể tiên đoán được nhiều tính chất hóa học như độ âm điện, bán kính nguyên tử, năng lượng ion hóa, và khả năng tạo thành các loại liên kết hóa học nhất định.
Hiểu biết về cấu hình electron
Bảng tuần hoàn giúp giải thích cấu hình electron của các nguyên tố, từ đó hiểu rõ hơn về nguyên nhân của các tính chất hóa học và vật lý của chúng.
Mối liên kết giữa các nguyên tố
Bảng tuần hoàn cho thấy mối liên kết giữa các nguyên tố trong cùng một nhóm hoặc chu kỳ, giúp phân tích và so sánh sự tương đồng và khác biệt giữa chúng.
Dự đoán phản ứng hóa học
Thông qua việc phân tích vị trí và tính chất của các nguyên tố trong bảng tuần hoàn, các nhà khoa học có thể dự đoán khả năng và loại phản ứng hóa học mà một nguyên tố có thể tham gia.
Dự đoán nguyên tố mới:
Trước khi một số nguyên tố được khám phá, bảng tuần hoàn đã tiên đoán được sự tồn tại và một số tính chất cơ bản của chúng dựa trên khoảng trống trong bảng.
Ứng dụng trong nhiều lĩnh vực

Bảng tuần hoàn được sử dụng rộng rãi trong nghiên cứu và giáo dục, từ hóa học, vật lý, đến khoa học vật liệu, y học và nhiều ngành khoa học khác, là công cụ không thể thiếu cho bất kỳ nhà khoa học nào.
Một vài nguyên tắc sắp xếp các nguyên tố trong bảng tuần hoàn
Sắp xếp theo số hiệu nguyên tử
Các nguyên tố trong bảng tuần hoàn được sắp xếp theo thứ tự tăng dần của số hiệu nguyên tử, tức là số lượng proton trong nhân nguyên tử. Số hiệu nguyên tử tăng dần từ trái sang phải trên mỗi hàng (chu kỳ) của bảng tuần hoàn.
Chu kỳ và nhóm
Chu Kỳ: Các hàng ngang trong bảng tuần hoàn được gọi là chu kỳ, phản ánh số lớp electron trong nguyên tử. Mỗi chu kỳ mới bắt đầu khi electron bắt đầu điền vào một lớp electron mới.
Nhóm: Các cột dọc được gọi là nhóm, phân loại các nguyên tố có số electron lớp vỏ ngoài cùng giống nhau, dẫn đến tính chất hóa học tương tự. Nhóm được chia thành nhóm chính (A) và nhóm phụ (B).
Cấu hình electron

Nguyên tố được sắp xếp sao cho cấu hình electron của chúng phản ánh một cách hợp lý qua các chu kỳ và nhóm. Cấu hình electron giúp xác định tính chất hóa học của nguyên tố và vị trí của chúng trong bảng tuần hoàn.
Khối s, p, d, và f
- Nguyên tố được sắp xếp vào các khối dựa trên electron cuối cùng được thêm vào orbital s, p, d, hay f. Điều này giúp phản ánh tính chất hóa học và cấu hình electron tương đối của các nguyên tố.
- Ví dụ, các nguyên tố khối s có electron cuối cùng được thêm vào orbital s, bao gồm các kim loại kiềm và kim loại kiềm thổ.
Tính chất hóa học
Các nguyên tố được sắp xếp sao cho những nguyên tố có tính chất hóa học tương tự nhau nằm cùng một nhóm. Điều này giúp dễ dàng tiên đoán tính chất của một nguyên tố dựa trên vị trí của nó trong nhóm.
Cách đọc bảng tuần hoàn
Đọc bảng tuần hoàn hóa học là kỹ năng cơ bản nhưng quan trọng, giúp hiểu và sử dụng thông tin về các nguyên tố hóa học một cách hiệu quả. Dưới đây là một vài hướng dẫn cách đọc bảng tuần hoàn:
Hiểu số hiệu nguyên tử
- Số hiệu nguyên tử, thường được hiển thị ở phần trên cùng của mỗi ô, cho biết số lượng proton trong nhân nguyên tử của nguyên tố. Số hiệu nguyên tử cũng tương ứng với số lượng electron trong nguyên tử ở trạng thái trung hòa.
Ký hiệu hóa học

- Ký hiệu hóa học, thường ở giữa ô, là cách viết tắt của tên nguyên tố, gồm một hoặc hai chữ cái, trong đó chữ cái đầu tiên viết hoa.
Khối lượng nguyên tử
- Khối lượng nguyên tử, thường được hiển thị ở phần dưới cùng của ô, là khối lượng trung bình của tất cả các đồng vị tự nhiên của nguyên tố, đơn vị là khối lượng nguyên tử (u).
Nhận biết chu kỳ và nhóm
- Chu Kỳ: Các hàng ngang trong bảng tuần hoàn được gọi là chu kỳ, từ 1 đến 7, phản ánh số lớp electron trong nguyên tử.
- Nhóm: Các cột dọc được gọi là nhóm, từ 1 đến 18, cho thấy các nguyên tố có số electron lớp vỏ ngoài cùng giống nhau và có tính chất hóa học tương tự.
Tìm hiểu tính chất hóa học dựa vào nhóm
- Nguyên tố trong cùng một nhóm (cột dọc) có tính chất hóa học tương tự nhau. Ví dụ, tất cả các nguyên tố trong nhóm 1 (kim loại kiềm) đều rất hoạt động hóa học và phản ứng mạnh với nước.
Khối s, p, d, và f
- Bảng tuần hoàn cũng được chia thành các khối dựa trên cấu hình electron của lớp ngoài cùng: khối s (nhóm 1 và 2), khối p (nhóm 13 đến 18), khối d (nhóm chuyển tiếp), và khối f (lanthanides and actinides).
Mẹo ghi nhớ bảng tuần hoàn hoá học
Theo dãy hoạt động hoá học của các kim loại
| Khi | Nào | Bạn | Cần | May | Áo | Giáp | Sắt | Nhìn | Sang | Phố | Hỏi | Cửa | Hàng | Á | Phi | Âu |
| K | Na | Ba | Ca | Mg | Al | Zn | Fe | Ni | Sn | Pb | H | Cu | Hg | Ag | Pt | Au |
Ghi nhớ các dãy theo nhóm bằng những câu có nghĩa
Nhóm IA: Lâu – nay – không – rảnh – coi – phim (Li – Na – K – Rb – Cs – Fr)
Nhóm IIA: Bé – mang – cây – súng – bắn – ruồi (Be – Mg – Ca – Sr – Ba – Ra)
Nhóm III: Bố Anh Gà In Tại Nhà (B,Al,Ga,In,Tl)
Nhóm IV: Chú Sĩ Gió Sóng Phở (C,Si,Ge,Sn,Pb)
Nhóm V: Nhớ Phải Ơn Sống Bền (N,P,As,Sb,Bi)
Nhóm VI: Ông Say Xỉn Té Phọt (O,S,Se,Te,Po)
Nhóm VII: Phải Chị Bé Yêu Anh (F,Cl,Br,I,At)
Nhóm VIII: Hãy Nếm Ăn Khúc Xương Rồng (He,Ne,Ar,Kr,Xe,Rn)
Mẹo ghi nhớ bảng tuần hoàn bằng thơ nhanh nhất
Cách nhớ các nguyên tố từ 1-20 qua thơ
H He
Li Be B C N O F Ne
Na Mg Al Si P S Cl Ar
K Ca
Hoàng Hôn
Lặn Bể Bắc Chợt Nhớ Ở Phương Nam
Nắng Mai Ánh Sương Phủ Song Cửa Ai
Không Cà
Cách nhớ các nguyên tố từ 21-30 qua thơ
Sc Ti V Cr Mn Fe Co Ni Cu Zn
Sáng Tối Vui Ca Múa Fải Có Nhạc Có Khèn
Bảng tuần hoàn hóa học là một công cụ vô cùng quan trọng trong hoá học, giúp chúng ta hiểu rõ hơn về cấu tạo nguyên tử, tính chất của các nguyên tố và mối liên hệ giữa chúng. Với một số mẹo ghi nhớ trên yeuhoahoc.edu.vn chúc các bạn học tập tốt ghi nhớ sâu và đạt kết quả cao trong học tập nhé!









