AgCl kết tủa màu gì - Khám phá chi tiết và các phản ứng hóa học
Trong hóa học, một trong những câu hỏi thường gặp là AgCl kết tủa màu gì?. AgCl, hay còn gọi là bạc clorua (Silver Chloride), là một hợp chất quan trọng trong nhiều phản ứng hóa học và có tính chất đặc trưng về màu sắc khi kết tủa
Trong hóa học, một trong những câu hỏi thường gặp là AgCl kết tủa màu gì?. AgCl, hay còn gọi là bạc clorua (Silver Chloride), là một hợp chất quan trọng trong nhiều phản ứng hóa học và có tính chất đặc trưng về màu sắc khi kết tủa. Bài viết này sẽ giúp bạn hiểu rõ về màu sắc kết tủa của AgCl, các phản ứng hóa học liên quan và ứng dụng của hợp chất này trong hóa học.
AgCl kết tủa màu gì?
AgCl, hay bạc clorua, khi kết tủa có màu trắng sữa. Khi ion bạc (Ag⁺) và ion clorua (Cl⁻) gặp nhau trong dung dịch, chúng sẽ tạo thành một chất rắn không tan trong nước, gọi là kết tủa AgCl. Quá trình này diễn ra thông qua phản ứng trao đổi ion, và kết quả là xuất hiện kết tủa trắng đặc trưng của bạc clorua.
Phản ứng hình thành AgCl kết tủa
\(Ag^+ (aq) + Cl^- (aq) \rightarrow AgCl (s)\)
Trong đó:
- Ag⁺ là ion bạc.
- Cl⁻ là ion clorua.
- AgCl là kết tủa bạc clorua màu trắng.

Tính chất hóa học của AgCl
AgCl là một muối không tan trong nước, và kết tủa AgCl màu trắng sẽ hình thành ngay lập tức khi có sự hiện diện của ion bạc (Ag⁺) và ion clorua (Cl⁻). Ngoài ra, AgCl còn có một số tính chất đặc biệt khác.
Độ tan thấp trong nước
AgCl rất ít tan trong nước, do đó khi hình thành trong dung dịch, nó sẽ xuất hiện dưới dạng chất rắn màu trắng. Độ tan của AgCl là khoảng 1.92×10−5 mol/L1.92 \times 10^{-5} \, \text{mol/L}1.92×10−5mol/L, điều này có nghĩa là chỉ có một lượng rất nhỏ AgCl có thể tan trong nước.
Nhạy cảm với ánh sáng
AgCl có một tính chất độc đáo là nhạy cảm với ánh sáng. Khi tiếp xúc với ánh sáng mặt trời hoặc tia UV, AgCl bị phân hủy và chuyển thành bạc kim loại (Ag) và khí clo (Cl₂). Phản ứng phân hủy này được biểu diễn như sau:
\(2Ag(s)+Cl2(g)2AgCl (s) \xrightarrow{ánh sáng} 2Ag (s) + Cl_2 (g)\)
Điều này giải thích tại sao sau một thời gian dài tiếp xúc với ánh sáng, kết tủa AgCl màu trắng sẽ chuyển sang màu xám đen, do sự hình thành của bạc kim loại trên bề mặt.
Phản ứng hòa tan trong dung dịch amoniac
Một trong những tính chất thú vị của AgCl là khả năng hòa tan trong dung dịch amoniac (NH₃). Khi cho AgCl kết tủa màu trắng vào dung dịch amoniac, AgCl sẽ tan tạo thành phức chất [Ag(NH₃)₂]⁺. Phản ứng này diễn ra như sau:
\(AgCl (s) + 2NH₃ (aq) \rightarrow [Ag(NH₃)_2]^+ (aq) + Cl^- (aq)\)
Phản ứng này cho thấy AgCl có thể chuyển thành dạng ion phức tan trong dung dịch, và đó là lý do tại sao nó có thể được loại bỏ hoặc xử lý trong môi trường amoniac.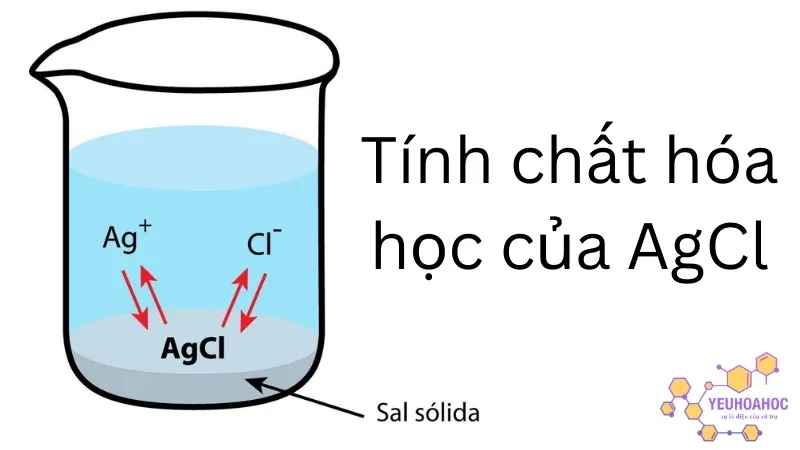
Các phản ứng hóa học liên quan đến AgCl
Bạc clorua (AgCl) là một hợp chất quan trọng trong nhiều phản ứng hóa học. Dưới đây là một số phản ứng phổ biến liên quan đến AgCl.
Phản ứng tạo AgCl từ dung dịch muối bạc và muối clorua
Như đã đề cập, khi dung dịch chứa ion bạc (Ag⁺) gặp dung dịch chứa ion clorua (Cl⁻), sẽ xảy ra phản ứng tạo thành kết tủa AgCl màu trắng:
\(AgNO_3 (aq) + NaCl (aq) \rightarrow AgCl (s) + NaNO_3 (aq)\)
Trong phản ứng này, AgNO₃ (bạc nitrat) và NaCl (natri clorua) là hai dung dịch phổ biến được sử dụng để tạo AgCl kết tủa. Sau phản ứng, AgCl sẽ kết tủa ra khỏi dung dịch dưới dạng chất rắn màu trắng.
Phản ứng phân hủy của AgCl dưới ánh sáng
Phản ứng phân hủy của AgCl dưới ánh sáng đã được đề cập ở trên. Điều này đặc biệt quan trọng trong ngành nhiếp ảnh truyền thống, nơi các hợp chất bạc halide (bao gồm AgCl) được sử dụng để tạo ra hình ảnh trên phim khi tiếp xúc với ánh sáng.
Phản ứng:
\(2AgCl (s) \xrightarrow{ánh sáng} 2Ag (s) + Cl_2 (g)\)
Phản ứng này tạo ra bạc kim loại màu đen, làm nền tảng cho quá trình tạo ảnh trên phim.
Phản ứng hòa tan AgCl trong dung dịch amoniac
AgCl có thể tan trong dung dịch amoniac tạo thành ion phức [Ag(NH₃)₂]⁺, cho phép bạc clorua được hòa tan. Đây là một phản ứng quan trọng trong phân tích hóa học, giúp xử lý AgCl trong một số phương pháp định lượng.
Phản ứng
\(AgCl (s) + 2NH₃ (aq) \rightarrow [Ag(NH₃)_2]^+ (aq) + Cl^- (aq)\)
Sau phản ứng, ion bạc tồn tại dưới dạng phức chất trong dung dịch và có thể được tách ra khỏi hệ thống.
Phản ứng của AgCl với axit mạnh
AgCl không tan trong axit loãng, tuy nhiên, trong môi trường axit mạnh như axit nitric (HNO₃) đậm đặc, nó có thể tham gia vào một số phản ứng hóa học. Tuy nhiên, đây không phải là phản ứng phổ biến trong môi trường thông thường mà thường xảy ra ở điều kiện thí nghiệm đặc biệt.
Ứng dụng của AgCl trong đời sống và khoa học
Với các tính chất đặc biệt của mình, AgCl được ứng dụng rộng rãi trong nhiều lĩnh vực khác nhau, từ công nghiệp đến khoa học nghiên cứu.
Ứng dụng trong ngành nhiếp ảnh
Trước khi công nghệ máy ảnh kỹ thuật số phát triển, các hợp chất bạc halide như AgCl đã được sử dụng rộng rãi trong nhiếp ảnh. AgCl nhạy cảm với ánh sáng, cho phép nó được sử dụng để tạo ảnh trên phim ảnh. Khi tiếp xúc với ánh sáng, AgCl sẽ phân hủy tạo ra bạc kim loại màu đen, từ đó tạo ra hình ảnh.
Ứng dụng trong y tế
Bạc và các hợp chất của bạc, bao gồm AgCl, có tính kháng khuẩn mạnh. Điều này khiến chúng được sử dụng trong các loại băng gạc y tế và sản phẩm khử khuẩn. AgCl giúp ngăn chặn sự phát triển của vi khuẩn và vi sinh vật, bảo vệ vết thương khỏi nhiễm trùng.
Ứng dụng trong phân tích hóa học
AgCl được sử dụng trong các phương pháp phân tích hóa học như chuẩn độ kết tủa, giúp xác định nồng độ của ion clorua trong các mẫu dung dịch. Trong phương pháp này, dung dịch bạc nitrat (AgNO₃) được thêm vào mẫu, và AgCl kết tủa sẽ được hình thành. Lượng kết tủa AgCl có thể được đo lường để tính toán nồng độ clorua trong mẫu.
AgCl kết tủa màu trắng là một hợp chất quan trọng trong nhiều phản ứng hóa học, đặc biệt là trong phân tích hóa học và ứng dụng y tế. AgCl có các tính chất đặc trưng như độ tan thấp, nhạy cảm với ánh sáng và khả năng tan trong dung dịch amoniac. Các phản ứng hóa học liên quan đến AgCl không chỉ giúp chúng ta hiểu rõ hơn về cách thức hoạt động của các ion trong dung dịch mà còn mở ra nhiều ứng dụng trong đời sống, từ nhiếp ảnh truyền thống đến y tế và nghiên cứu khoa học.
Bài Viết Liên Quan
P.GS Kiều Oanh với kinh nghiệm hơn 20 năm trong vực hóa học và giảng dạy cùng với niềm đam mê nghiên cứu khoa học. Các bài viết của tác giả mang tính chuyên sâu, cung cấp thông tin dễ hiểu, chính xác và cập nhật. Với phong cách diễn đạt rõ ràng, bà giúp người đọc nắm bắt các khái niệm khoa học một cách dễ dàng và sinh động.







