Chất tan là một khái niệm quan trọng trong hóa học và có mặt ở khắp mọi nơi trong cuộc sống, từ muối trong nước, đường trong trà cho đến khí oxy hòa tan trong đại dương. Hiểu rõ về chất tan và cách chúng hòa tan giúp giải thích nhiều hiện tượng khoa học và ứng dụng trong các ngành công nghiệp như dược phẩm, thực phẩm, và công nghệ hóa học. Tìm hiểu về chất tan không chỉ làm sáng tỏ các khía cạnh của thế giới tự nhiên mà còn mở ra nhiều tiềm năng ứng dụng thực tiễn thú vị.
Chất tan là chất gì?
Chất tan là một chất có thể hòa tan trong một dung môi để tạo thành một dung dịch đồng nhất. Trong dung dịch, chất tan là thành phần có mặt ở lượng ít hơn so với dung môi. Chất tan phân tán đều trong dung môi ở cấp độ phân tử hoặc ion, khiến chúng không thể phân biệt được bằng mắt thường và tạo thành một hỗn hợp đồng nhất.
Xem thêm: Dung môi là gì?
Ví dụ quen thuộc nhất về chất tan là muối hoặc đường khi hòa tan trong nước. Trong trường hợp này, muối hoặc đường là chất tan, và nước là dung môi. Khi muối hoặc đường hòa tan trong nước, chúng sẽ bị phân tách thành các ion hoặc phân tử nhỏ, và phân tán đều khắp trong dung dịch, tạo thành một hỗn hợp không thể phân biệt được.
Đặc điểm của chất tan
Phân tử hoặc ion nhỏ: Trong quá trình hòa tan, các phân tử hoặc ion của chất tan phân tán và tương tác với các phân tử dung môi. Điều này giúp dung dịch đồng nhất, không có phân lớp hay tách biệt giữa chất tan và dung môi.
Không thể phân biệt bằng mắt thường: Khi chất tan hòa tan hoàn toàn, nó trở nên vô hình trong dung dịch. Điều này có nghĩa là dung dịch trông sẽ đồng nhất và trong suốt (nếu cả chất tan và dung môi đều không có màu).
Thường có khối lượng nhỏ hơn so với dung môi: Để được xem là chất tan, thường khối lượng của nó nhỏ hơn so với dung môi trong dung dịch. Nếu chất tan có mặt với lượng lớn hơn, nó sẽ được gọi là dung môi chính.
Phụ thuộc vào loại dung môi và điều kiện hòa tan: Không phải mọi chất đều có thể tan trong mọi dung môi. Ví dụ, dầu không tan trong nước vì bản chất phân tử của dầu và nước không tương thích, nhưng dầu lại dễ tan trong dung môi hữu cơ như hexan hoặc xăng.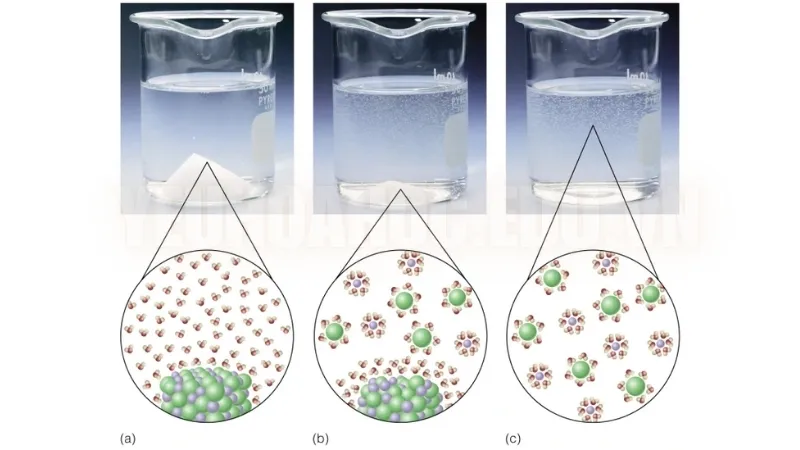
Tính chất của chất tan
Chất tan có nhiều tính chất quan trọng quyết định khả năng và cách thức hòa tan trong dung môi, cũng như ứng dụng của chúng trong thực tế.
Tính chất lý hóa của chất tan
Chất tan có một số tính chất lý hóa, như:
- Độ tan: Khả năng hòa tan trong một dung môi cụ thể ở một nhiệt độ nhất định.
- Điểm nóng chảy: Nhiệt độ mà chất tan chuyển từ trạng thái rắn sang lỏng.
- Điểm sôi: Nhiệt độ mà chất tan chuyển từ lỏng sang khí.
Các tính chất này giúp xác định cách thức hòa tan của chất tan và có thể ảnh hưởng đến ứng dụng của nó trong các lĩnh vực như sản xuất thuốc, thực phẩm, và hóa chất.
Độ tan của chất tan
Độ tan là lượng chất tan tối đa có thể hòa tan trong một lượng dung môi nhất định để tạo thành dung dịch bão hòa ở một nhiệt độ cụ thể. Độ tan phụ thuộc vào các yếu tố như loại chất tan, dung môi, nhiệt độ, và áp suất. Ví dụ, muối ăn có độ tan cao trong nước nhưng lại ít tan trong dầu. Chất tan được phân loại dựa vào độ tan của chúng, chẳng hạn như:
- Chất tan tan nhiều: Những chất có độ tan cao, dễ hòa tan trong dung môi.
- Chất tan tan ít: Những chất có độ tan thấp, khó hòa tan trong dung môi.
Độ tan và dung môi
Mối quan hệ giữa độ tan của chất tan và dung môi rất quan trọng trong nhiều ứng dụng. Các dung môi phân cực như nước hòa tan tốt các chất tan phân cực và ion (như muối, đường), trong khi các dung môi không phân cực (như dầu) hòa tan tốt các chất không phân cực. Việc chọn đúng dung môi giúp hòa tan chất tan một cách hiệu quả, ứng dụng trong các ngành công nghiệp thực phẩm, dược phẩm, hóa chất.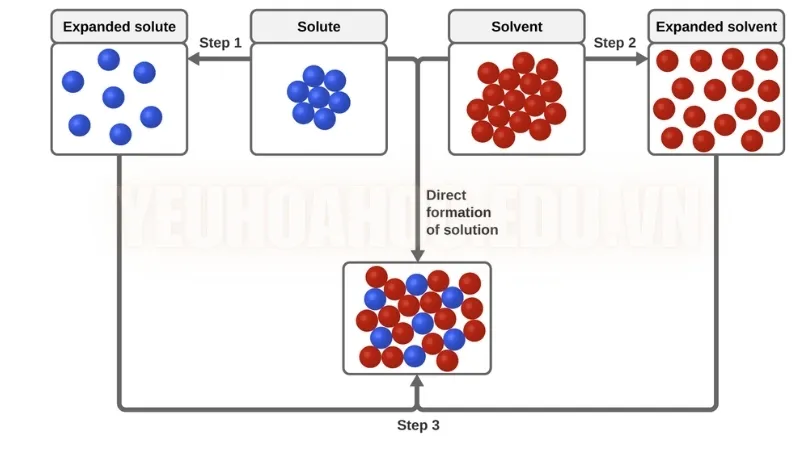
Cơ chế hòa tan của chất tan
Quá trình hòa tan xảy ra khi các phân tử hoặc ion của chất tan tương tác với các phân tử của dung môi một cách hiệu quả. Những tương tác này phải đủ mạnh để phá vỡ lực liên kết giữa các phân tử hoặc ion trong chất tan, khiến chúng phân tán trong dung môi.
Xem thêm: Các liên kết ion
- Đối với chất tan ion (như muối): Khi muối như NaCl hòa tan trong nước, các phân tử nước bao quanh các ion Na⁺ và Cl⁻, tách chúng khỏi tinh thể muối và phân tán đều trong nước.
- Đối với chất tan phân tử (như đường): Các phân tử đường tách rời khỏi nhau và phân tán trong dung dịch mà không bị ion hóa.
Các loại chất tan
Chất tan có thể ở ba dạng chính: khí, lỏng và rắn. Dựa trên trạng thái của chất tan và dung môi, chúng ta có các loại dung dịch khác nhau. Hỗn hợp đồng nhất là hỗn hợp mà các thành phần phân bố đều và không phân biệt được bằng mắt thường (chẳng hạn như nước muối), còn hỗn hợp không đồng nhất là nơi các thành phần không trộn lẫn hoàn toàn và có thể phân biệt được (như nước với dầu).
Chất tan dạng khí
Chất tan dạng khí có thể hòa tan vào cả dung môi khí, lỏng và rắn, tạo ra các loại dung dịch khác nhau:
- Khí trong khí: Khi cả chất tan và dung môi đều là khí, chúng tạo thành hỗn hợp khí đồng nhất. Ví dụ, không khí là một dung dịch khí trong đó nitơ đóng vai trò là dung môi, còn oxy và các khí khác (như CO₂, argon) là chất tan.
- Khí trong lỏng: Chất tan dạng khí có thể hòa tan trong dung môi lỏng, ví dụ như oxy hòa tan trong nước giúp sinh vật dưới nước hô hấp, hoặc carbon dioxide (CO₂) hòa tan trong nước để tạo ra nước có gas.
- Khí trong rắn: Khí cũng có thể tan vào các kim loại, như hydro có thể hòa tan trong kim loại paladi. Ở đây, paladi là dung môi, còn hydro là chất tan.
Chất tan dạng lỏng
Khi chất tan là chất lỏng, nó có thể hòa tan vào dung môi lỏng hoặc dung môi rắn:
- Lỏng trong lỏng: Trong trường hợp này, cả chất tan và dung môi đều ở dạng lỏng, tạo ra một dung dịch đồng nhất. Ví dụ, cồn etanol hòa tan trong nước tạo thành đồ uống có cồn, trong đó cả hai chất đều là chất lỏng và có thể hòa tan dễ dàng vào nhau.
- Lỏng trong rắn: Một số chất tan dạng lỏng có thể hòa tan trong dung môi rắn. Ví dụ như thủy ngân hòa tan trong vàng để tạo thành hợp chất gọi là hỗn hống. Hoặc nước có thể thẩm thấu vào một số chất rắn như muối hoặc đường, tạo ra các chất rắn ẩm. Tuy nhiên, lưu ý rằng chất tan dạng lỏng không thể hòa tan trong dung môi khí, vì khí không thể giữ chất tan dạng lỏng.
Chất tan dạng rắn
Chất tan dạng rắn thường có thể hòa tan vào dung môi lỏng hoặc rắn, nhưng không thể tan trong khí:
- Rắn trong lỏng: Một ví dụ phổ biến là muối hoặc đường hòa tan trong nước để tạo thành dung dịch. Trong trường hợp này, muối hoặc đường là chất tan, còn nước là dung môi.
- Rắn trong rắn: Chất tan dạng rắn cũng có thể hòa tan trong dung môi rắn để tạo thành hợp kim hoặc hỗn hợp rắn đồng nhất. Ví dụ, thép là dung dịch của nguyên tử cacbon tan trong mạng tinh thể của nguyên tử sắt. Các hợp kim như đồng thau cũng là ví dụ của dung dịch rắn trong rắn.

Ví dụ về chất tan
Muối trong nước
Khi cho một thìa muối vào cốc nước, chúng ta tạo ra một dung dịch, trong đó muối (NaCl) là chất tan và nước (H₂O) là dung môi. Muối là một hợp chất ion gồm các ion Na⁺ (natri) và Cl⁻ (clorua). Khi hòa tan, các phân tử nước, với đầu oxy mang điện âm và đầu hydro mang điện dương, sẽ tương tác với các ion của muối. Đầu âm của phân tử nước hút Na⁺, trong khi đầu dương hút Cl⁻. Lực hút này kéo các ion Na⁺ và Cl⁻ ra khỏi cấu trúc tinh thể ban đầu của muối và phân tán chúng đều trong nước, tạo ra một dung dịch đồng nhất.
Diện tích bề mặt của muối cũng ảnh hưởng đến tốc độ hòa tan. Nếu dùng muối thô (hạt lớn), quá trình hòa tan sẽ chậm hơn do diện tích bề mặt tiếp xúc ít hơn. Ngược lại, muối mịn hơn với diện tích bề mặt lớn sẽ hòa tan nhanh chóng, vì các ion có thể tiếp xúc với nước nhiều hơn. Khi muối hòa tan hoàn toàn, ta không còn thấy muối ở đáy cốc nữa do nó đã được phân tán đều trong nước.
Đường trong nước
Khi đường hòa tan trong nước, quá trình này tương tự như muối, nhưng cơ chế khác một chút. Đường không phải là hợp chất ion như muối mà là phân tử có các nhóm OH (hydroxyl) phân cực. Các nhóm OH này có các cực dương và cực âm tự nhiên, tương tác với các phân tử nước. Nhờ đó, nước kéo các phân tử đường ra khỏi cấu trúc ban đầu, phân tán chúng đều trong dung dịch.
Việc đường có thể hòa tan hoàn toàn trong nước rất quan trọng cho quá trình trao đổi chất của tế bào. Đường hòa tan trong tế bào cho phép tế bào sử dụng năng lượng và thực hiện các chức năng khác. Ngoài ra, tế bào có thể kiểm soát lượng phân tử đường và các chất khác để duy trì cân bằng độ pH, hỗ trợ hoạt động tế bào.
Oxy trong nước biển
Oxy là một chất tan dạng khí, đóng vai trò quan trọng trong đại dương. Các sinh vật biển, từ các sinh vật nhỏ đến cá lớn, đều cần oxy hòa tan trong nước để hô hấp. Oxy tồn tại dưới dạng phân tử O₂ phân cực, tương thích với các phân tử nước phân cực, nên nước có thể hút oxy vào.
Khi sóng biển và các dòng nước khuấy động không khí, oxy sẽ khuếch tán vào nước, cung cấp cho sinh vật biển. Tuy nhiên, đôi khi oxy bị tiêu thụ nhanh hơn lượng oxy mới khuếch tán vào nước. Điều này xảy ra khi có dòng chất dinh dưỡng dư thừa từ con người chảy vào, dẫn đến tảo phát triển quá mức. Khi tảo chết, vi khuẩn tiêu thụ oxy để phân hủy chúng, gây ra tình trạng thiếu oxy và tạo ra các “vùng chết” mà sinh vật biển không thể sống được.
Proton trong tế bào chất
Trong tế bào sống, các ion hydro (H⁺) hay còn gọi là proton là một loại chất tan quan trọng. Lượng proton trong tế bào quyết định độ axit của môi trường bên trong tế bào (tính pH). Các proton bị hút mạnh bởi các nguyên tử oxy của phân tử nước và không thể tự di chuyển qua màng tế bào. Thay vào đó, sự chênh lệch nồng độ proton tạo ra “động lực proton,” một dạng thế năng giúp vận chuyển các chất khác qua màng tế bào. Điều này rất quan trọng trong việc duy trì cân bằng nội môi của tế bào và hỗ trợ quá trình trao đổi chất.
Quá trình hòa tan chất tan
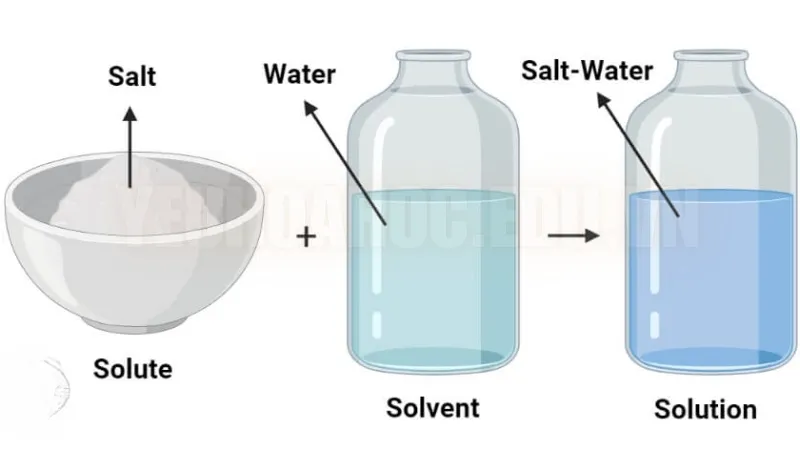
Quá trình hòa tan là khi các phân tử hoặc ion của chất tan (như muối, đường) phân tán đều trong dung môi (như nước) để tạo thành một dung dịch đồng nhất. Khi hòa tan, các phân tử chất tan sẽ bị tách rời và phân tán trong dung môi nhờ các lực tương tác giữa chúng với các phân tử của dung môi.
Khi một chất tan (chẳng hạn như muối) được thêm vào dung môi (như nước), các phân tử của dung môi bắt đầu tương tác với các phân tử hoặc ion của chất tan. Trong trường hợp muối (NaCl), các phân tử nước bao quanh các ion Na⁺ và Cl⁻, tách chúng ra khỏi cấu trúc tinh thể ban đầu và giúp chúng phân tán đều trong nước. Quá trình này được duy trì bởi lực hút giữa các phân tử dung môi và các phân tử chất tan, dẫn đến một dung dịch đồng nhất không phân lớp.
Các yếu tố ảnh hưởng đến quá trình hòa tan
Quá trình hòa tan có thể diễn ra nhanh hay chậm, nhiều hay ít, phụ thuộc vào các yếu tố sau đây:
Nhiệt độ
Nhiệt độ là yếu tố quan trọng ảnh hưởng đến độ hòa tan của chất tan. Khi nhiệt độ tăng, động năng của các phân tử dung môi tăng lên, làm cho chúng di chuyển nhanh hơn và tạo ra lực va chạm mạnh hơn với các phân tử chất tan. Điều này giúp chất tan tan nhanh hơn. Ví dụ, đường tan nhanh hơn trong nước nóng so với nước lạnh. Tuy nhiên, đối với một số chất khí tan trong dung môi lỏng, độ tan có thể giảm khi nhiệt độ tăng.
Áp suất
Áp suất ảnh hưởng chủ yếu đến độ hòa tan của chất tan dạng khí. Khi áp suất tăng, các phân tử khí bị nén lại gần nhau hơn, giúp chúng dễ dàng hòa tan trong dung môi lỏng. Ví dụ, trong nước ngọt có ga, CO₂ được hòa tan vào nước nhờ áp suất cao. Khi mở nắp chai, áp suất giảm, CO₂ sẽ thoát ra ngoài, tạo ra bong bóng khí.
Tính chất của dung môi
Mỗi dung môi có khả năng hòa tan các chất khác nhau tùy thuộc vào tính chất hóa học của nó. Ví dụ, nước là dung môi phân cực nên dễ dàng hòa tan các chất phân cực hoặc ion như muối và đường. Ngược lại, dầu là dung môi không phân cực, chỉ hòa tan tốt các chất không phân cực như dầu hoặc các chất béo. Do đó, khả năng hòa tan phụ thuộc vào sự tương thích về tính chất giữa chất tan và dung môi.
Kích thước hạt
Kích thước hạt của chất tan cũng ảnh hưởng đến tốc độ hòa tan. Các hạt nhỏ có diện tích bề mặt tiếp xúc với dung môi lớn hơn, giúp chúng hòa tan nhanh hơn. Ví dụ, muối mịn hòa tan nhanh hơn muối hạt thô vì có diện tích tiếp xúc nhiều hơn với dung môi.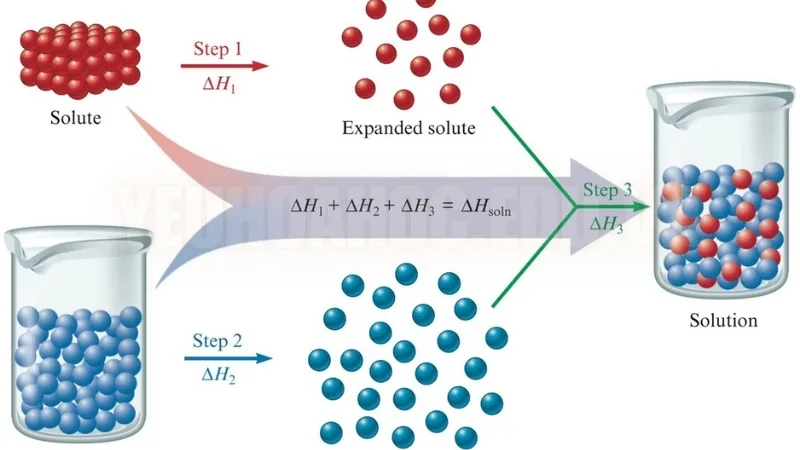
Ứng dụng của chất tan
Độ tan đóng vai trò quan trọng trong nhiều lĩnh vực thực tế như dược phẩm, thực phẩm và công nghiệp hóa chất.
Trong sản xuất thuốc, độ tan của các thành phần hoạt chất ảnh hưởng đến khả năng hấp thụ của thuốc vào cơ thể. Để thuốc phát huy tác dụng, hoạt chất cần hòa tan trong các dung môi sinh học như nước hoặc dầu để có thể đi qua màng tế bào vào máu. Độ tan cũng cho phép điều chỉnh liều lượng và tốc độ giải phóng thuốc, giúp kiểm soát tác dụng của thuốc từ ngắn hạn đến kéo dài. Các kỹ thuật như viên sủi hay công nghệ nano được sử dụng để tăng cường độ tan của hoạt chất, giúp thuốc hấp thụ nhanh chóng và hiệu quả hơn.
Trong chế biến thực phẩm, độ tan của đường, muối và các chất phụ gia ảnh hưởng trực tiếp đến hương vị và cấu trúc sản phẩm. Ví dụ, đường cần tan đều trong đồ uống để tạo vị ngọt đồng nhất. Độ tan cũng giúp giữ cho thực phẩm ổn định hơn về kết cấu, chẳng hạn như trong nước sốt hoặc đồ hộp. Nhờ đó, sản phẩm duy trì chất lượng ổn định trong thời gian dài.
Trong công nghiệp hóa chất, độ tan giúp kiểm soát các phản ứng hóa học khi pha chế dung dịch hoặc sản xuất hóa chất. Độ tan phù hợp đảm bảo phản ứng diễn ra hiệu quả, tạo ra các sản phẩm đạt chất lượng mong muốn. Nhờ ứng dụng của độ tan, các sản phẩm y tế, thực phẩm và hóa chất không chỉ có chất lượng ổn định mà còn đạt hiệu quả cao khi sử dụng.
Chất tan đóng vai trò thiết yếu trong cả khoa học và đời sống, giúp tạo nên các sản phẩm hữu ích và giải đáp nhiều câu hỏi về thiên nhiên và công nghệ. Từ quá trình hòa tan đến ứng dụng trong thực tế, kiến thức về chất tan mang lại những hiểu biết sâu sắc, ứng dụng hiệu quả cho nghiên cứu, sản xuất và phát triển công nghệ. Hiểu rõ chất tan là bước quan trọng để khám phá những tiềm năng mới và đáp ứng nhu cầu cuộc sống hiện đại.









