Hóa học hữu cơ nghiên cứu các hợp chất chứa carbon, là nền tảng của nhiều quá trình sinh học và công nghiệp. Tìm hiểu về cấu trúc, tính chất và phản ứng của các hợp chất hữu cơ để ứng dụng vào cuộc sống. Bài viết này, yeuhoahoc.edu.vn sẽ khám phá các khía cạnh chính của hóa học hữu cơ.
Khái niệm về hóa học hữu cơ
Hóa học hữu cơ là một ngành khoa học chuyên nghiên cứu về cấu trúc, tính chất, thành phần và phản ứng hóa học của các hợp chất hữu cơ và vật liệu hữu cơ. Nói cách khác, nó tập trung vào các hợp chất chứa cacbon, ngoại trừ một số trường hợp ngoại lệ như CO, CO2, muối cacbonat và cacbua kim loại.
Đặc điểm của hợp chất hữu cơ:
- Bắt buộc phải chứa nguyên tử Cacbon (C) trong thành phần của hợp chất.
- Hầu hết các hợp chất hữu cơ chứa cacbon và hydro, nhưng chúng cũng có thể bao gồm bất kỳ số nguyên tố nào khác (ví dụ: nitơ, oxy, halogen, phốt pho, silic, lưu huỳnh).
- Có sự đa dạng về cấu tạo và tính chất do khả năng liên kết đa dạng của nguyên tử cacbon.
- Dễ cháy.
Vai trò của hóa học hữu cơ:
- Hóa học hữu cơ đóng vai trò quan trọng trong nhiều lĩnh vực khác nhau của đời sống, bao gồm:
- Dược phẩm: Hầu hết các loại thuốc đều là hợp chất hữu cơ.
- Vật liệu: Nhựa, cao su, sợi tổng hợp,… đều là những vật liệu hữu cơ.
- Thực phẩm: Các chất dinh dưỡng thiết yếu như protein, carbohydrate, lipid,… đều là hợp chất hữu cơ.
- Nông nghiệp: Phân bón, thuốc trừ sâu, thuốc kích thích sinh trưởng,… đều là những hợp chất hữu cơ.
- Hóa học sinh học: Hóa học hữu cơ đóng vai trò quan trọng trong việc nghiên cứu cấu trúc và chức năng của các phân tử sinh học như protein, DNA, RNA,…
Phân loại hợp chất hữu cơ
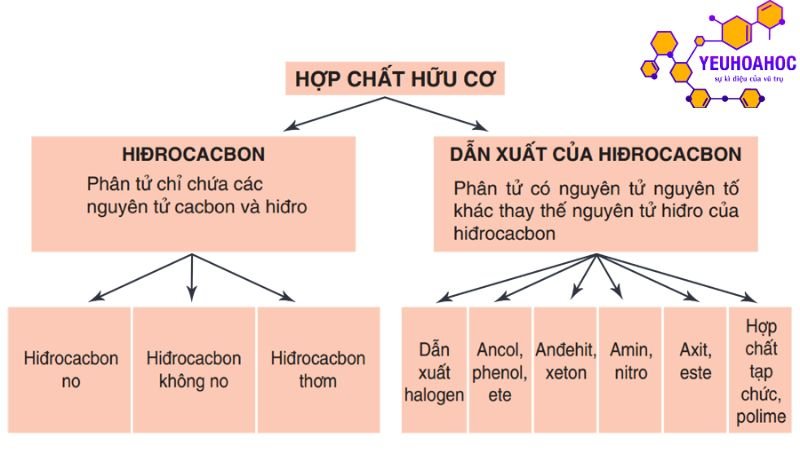
Phân loại dựa trên cấu tạo mạch cacbon:
- Mạch hở: Mạch cacbon trong phân tử không tạo thành vòng.
- Mạch vòng: Mạch cacbon trong phân tử tạo thành vòng.
Phân loại dựa trên nhóm chức năng:
- Hidrocacbon: Chỉ chứa nguyên tử cacbon và hiđro.
Hidrocacbon no (ankan): Mạch cacbon no, chỉ có liên kết đơn C-C và C-H.
Hidrocacbon không no: Mạch cacbon không no, có chứa liên kết đôi C=C hoặc liên kết ba C≡C.
Anken: Chứa 1 liên kết đôi C=C.
Ankin: Chứa 1 liên kết ba C≡C.
Dien: Chứa nhiều liên kết đôi C=C.
- Dẫn xuất hidrocacbon: Chứa nguyên tử cacbon, hiđro và ít nhất 1 nguyên tố khác (O, N, halogen,…).
Dẫn xuất halogen: Thay thế 1 hoặc nhiều nguyên tử hiđro trong hidrocacbon bằng nguyên tử halogen (F, Cl, Br, I).
Ancol: Nhóm chức hydroxyl (-OH) liên kết với nguyên tử cacbon no.
Phenol: Nhóm chức hydroxyl (-OH) liên kết với nguyên tử cacbon thơm.
Anđehit: Nhóm chức carbonyl (C=O) ở đầu mạch cacbon.
Xeton: Nhóm chức carbonyl (C=O) ở giữa mạch cacbon.
Axit cacbonxilic: Nhóm chức cacboxyl (-COOH).
Este: Nhóm chức este (-COO-) được tạo bởi axit cacbonxilic và ancol.
Cấu tạo và liên kết hóa học trong hợp chất hữu cơ
Khái niệm về cấu tạo hóa học của hợp chất hữu cơ:
Cấu tạo hóa học của hợp chất hữu cơ là trật tự liên kết giữa các nguyên tử trong phân tử, thể hiện thành phần, cấu tạo mạch cacbon và nhóm chức năng của hợp chất.
Các dạng liên kết hóa học tồn tại trong hợp chất hữu cơ
- Liên kết cộng hóa trị:
- Là loại liên kết được hình thành do sự dùng chung electron giữa các nguyên tử.
- Là dạng liên kết phổ biến nhất trong hợp chất hữu cơ.
- Có thể chia thành hai loại:
- Liên kết cộng hóa trị đơn (σ): Do một cặp electron dùng chung tạo thành.
- Ví dụ: Liên kết C-H, C-C trong các hidrocacbon no.
- Liên kết cộng hóa trị bội (π): Do nhiều cặp electron dùng chung tạo thành.
- Ví dụ: Liên kết C=C trong các hidrocacbon không no.
- Liên kết cộng hóa trị đơn (σ): Do một cặp electron dùng chung tạo thành.
- Liên kết ion:
- Là loại liên kết được hình thành do sự hút nhau giữa các ion mang điện tích trái dấu.
- Ít phổ biến trong hợp chất hữu cơ.
- Ví dụ: Muối hữu cơ như CH3COONa (Natri axetat).
Ảnh hưởng của cấu tạo và liên kết hóa học đến tính chất của hợp chất hữu cơ:
- Cấu tạo mạch cacbon:
- Mạch cacbon hở:
- Dễ cháy, dễ bay hơi.
- Phản ứng thế dễ xảy ra.
- Mạch cacbon vòng:
- Ổn định hơn, khó cháy, khó bay hơi hơn.
- Phản ứng cộng dễ xảy ra.
- Mạch cacbon hở:
- Nhóm chức năng:
- Quyết định tính chất hóa học cơ bản của hợp chất hữu cơ.
- Ví dụ:
- Nhóm chức hydroxyl (-OH) trong ancol và phenol có tính axit yếu.
- Nhóm chức carbonyl (C=O) trong anđehit, xeton, axit cacbonxilic và este có tính oxi hóa.
- Liên kết cộng hóa trị:
- Ảnh hưởng đến độ bền, nhiệt độ sôi, nhiệt độ nóng chảy của hợp chất hữu cơ.
- Ví dụ: Liên kết C=C bền hơn liên kết C-C, do đó hợp chất có liên kết C=C có nhiệt độ sôi cao hơn.
Danh pháp hóa học của hợp chất hữu cơ
Danh pháp quốc tế IUPAC (International Union of Pure and Applied Chemistry):
- Là hệ thống danh pháp quốc tế, được ưa chuộng trong nghiên cứu khoa học và xuất bản.
- Dựa trên cấu tạo hóa học của hợp chất, sử dụng các tiền tố, tiếp tố và số chỉ vị trí để mô tả mạch cacbon, nhóm chức năng và các thay thế.
- Ví dụ:
- Etan (CH3CH3): Hệ thống IUPAC: Đimetyl metan
- Propanol (CH3CH2CH2OH): Hệ thống IUPAC: 1-Propanol
- Axit axetic (CH3COOH): Hệ thống IUPAC: Etanđioic axit
- Ưu điểm:
- Tên gọi khoa học, chính xác, dễ hiểu.
- Dễ dàng tra cứu thông tin về hợp chất.
- Nhược điểm:
- Có thể dài, phức tạp đối với các hợp chất có cấu tạo phức tạp.
- Không thường xuyên được sử dụng trong cuộc sống hàng ngày.
Danh pháp thường gặp
- Là hệ thống danh pháp đơn giản, dễ nhớ, được sử dụng trong đời sống thường ngày.
- Dựa trên nguồn gốc, tính chất hoặc ứng dụng của hợp chất.
- Ví dụ:
- Ưu điểm:
- Ngắn gọn, dễ nhớ, dễ sử dụng.
- Phù hợp với đời sống thường ngày.
- Nhược điểm:
- Không chính xác, không khoa học.
- Có thể gây nhầm lẫn cho các hợp chất có tên gọi giống nhau.
Hướng dẫn cách đặt tên cho các hợp chất hữu cơ thuộc các nhóm chức năng khác nhau:
- Hidrocacbon:
- Xác định mạch cacbon: mạch hở hay mạch vòng.
- Xác định số lượng nguyên tử cacbon trong mạch.
- Sử dụng tiền tố và tiếp tố tương ứng để đặt tên.
- Ví dụ:
Etan (CH3CH3): Mạch hở, 2 nguyên tử cacbon, tiền tố “e”, tiếp tố “an”. Tên gọi: Etan.
Cyclohexan (C6H12): Mạch vòng, 6 nguyên tử cacbon, tiếp tố “an”. Tên gọi: Cyclohexan.
- Dẫn xuất hidrocacbon:
- Xác định mạch cacbon và nhóm chức năng.
- Sử dụng tên của hidrocacbon gốc và tên của nhóm chức năng.
- Xác định vị trí của nhóm chức năng bằng số chỉ vị trí.
- Ví dụ:
Etanol (CH3CH2OH): Etan (gốc hidrocacbon) + ol (nhóm chức năng ancol). Tên gọi: Etanol.
Axit axetic (CH3COOH): Etan (gốc hidrocacbon) + oic (nhóm chức năng axit cacbonxilic) + axit (loại hợp chất). Tên gọi: Axit axetic.
- Hợp chất thơm:
- Xác định tên gọi của vòng benzen.
- Xác định các chất thay thế trên vòng benzen và vị trí của chúng.
- Sử dụng tiền tố và tiếp tố tương ứng để đặt tên cho các chất thay thế.
- Ví dụ:
- Toluen (CH3C6H5): Benzen (vòng benzen) + metyl (chất thay thế ở vị trí 1). Tên gọi: Toluen.
- Xilen (CH3(CH3)C6H3): Benzen (vòng benzen) + 2 metyl (chất thay thế ở vị trí 1 và 4). Tên gọi: Xilen.
Ứng dụng của hóa học hữu cơ

Thực phẩm
- Hầu hết các chất dinh dưỡng thiết yếu cho cơ thể con người như protein, carbohydrate, lipid đều là hợp chất hữu cơ.
- Các chất phụ gia thực phẩm, chất tạo màu, chất tạo hương vị,… cũng là hợp chất hữu cơ.
- Ví dụ:
- Protein: Thịt, cá, trứng, sữa,…
- Carbohydrate: Gạo, mì, bánh mì, trái cây,…
- Lipid: Dầu ăn, mỡ động vật,…
- Chất phụ gia thực phẩm: Muối, đường, chất bảo quản,…
- Chất tạo màu: Beta caroten (màu vàng cam), chlorophyll (màu xanh lá cây),…
- Chất tạo hương vị: Vanillin (hương vani), ethyl acetate (hương trái cây),…
Y học
- Hầu hết các loại thuốc hiện nay đều là hợp chất hữu cơ.
- Ví dụ:
- Kháng sinh: Penicillin, amoxicillin,…
- Thuốc giảm đau: Paracetamol, ibuprofen,…
- Thuốc tim mạch: Aspirin, warfarin,…
- Thuốc chống ung thư: Taxol, cisplatin,…
- Hóa học hữu cơ cũng đóng vai trò quan trọng trong chẩn đoán và điều trị bệnh tật.
- Ví dụ:
- Xét nghiệm máu: Xét nghiệm lượng đường trong máu, cholesterol,…
- Chụp X-quang: Sử dụng chất cản quang có chứa nguyên tử iodine.
- Liệu pháp gen: Sử dụng virus để đưa gen mong muốn vào cơ thể.
Công nghiệp
- Hóa học hữu cơ cung cấp nguyên liệu cho nhiều ngành công nghiệp quan trọng như:
- Công nghiệp hóa chất: Sản xuất nhựa, cao su, xơ tổng hợp, dung môi,…
- Công nghiệp dược phẩm: Sản xuất thuốc, hóa chất sinh học,…
- Công nghiệp thực phẩm: Sản xuất phụ gia thực phẩm, chất tạo màu, chất tạo hương vị,…
- Công nghiệp mỹ phẩm: Sản xuất kem dưỡng da, son môi, nước hoa,…
- Ví dụ:
- Nhựa: Polyethylene, polypropylene, PVC,…
- Cao su: Cao su tổng hợp, cao su thiên nhiên,…
- Xơ tổng hợp: Polyester, nylon, acrylic,…
- Dung môi: Acetone, ethanol, methanol,…
Nông nghiệp
- Hóa học hữu cơ cung cấp các sản phẩm thiết yếu cho ngành nông nghiệp như:
- Phân bón: Phân đạm, phân lân, phân kali,…
- Thuốc trừ sâu: DDT, chlorpyrifos,…
- Thuốc diệt cỏ: Glyphosate, 2,4-D,…
- Chất kích thích sinh trưởng: Auxin, gibberellin,…
- Ví dụ:
- Phân đạm: Urea, ammonium sulfate,…
- Phân lân: Superphosphate, triple superphosphate,…
- Phân kali: Muriate of potash, potassium sulfate,…
- Thuốc trừ sâu: DDT, chlorpyrifos,…
- Thuốc diệt cỏ: Glyphosate, 2,4-D,…
- Chất kích thích sinh trưởng: Auxin, gibberellin,…
Hóa học hữu cơ không chỉ là nền tảng của nhiều ngành khoa học mà còn ứng dụng rộng rãi trong công nghiệp và đời sống. Việc nắm vững các kiến thức về hóa học hữu cơ sẽ mở ra nhiều cơ hội nghiên cứu và ứng dụng thực tiễn.









