Khám phá thế giới diệu kỳ của muối – từ gia vị quen thuộc đến hợp chất hóa học đa năng! Bài viết này sẽ cung cấp cho bạn kiến thức toàn diện về muối, bao gồm khái niệm, phân loại, tính chất, ứng dụng và tác hại. Hãy cùng chúng tôi tìm hiểu về vai trò thiết yếu của muối trong đời sống và cách sử dụng muối hợp lý để bảo vệ sức khỏe và môi trường.
Khái niệm về muối

Định nghĩa:
Theo hóa học, muối là hợp chất ion được hình thành từ cation kim loại và anion gốc axit. Nói cách khác, muối là sản phẩm của phản ứng trung hòa axit – bazơ, trong đó cation của bazơ kết hợp với anion của axit để tạo thành hợp chất có tính chất trung hòa về điện.
Ví dụ:
- Muối ăn (NaCl): Natri (cation kim loại) kết hợp với Clorua (anion gốc axit)
- Canxi sunfat (CaSO4): Canxi (cation kim loại) kết hợp với Sunfat (anion gốc axit)
- Kali nitrat (KNO3): Kali (cation kim loại) kết hợp với Nitrat (anion gốc axit)
Đặc điểm:
- Muối thường ở trạng thái rắn, dạng tinh thể, có màu trắng hoặc màu đặc trưng của cation/anion.
- Muối có vị mặn, tan trong nước tạo dung dịch dẫn điện.
- Muối có thể được hình thành từ nhiều cách khác nhau, bao gồm:
- Phản ứng trung hòa axit – bazơ
- Phản ứng trao đổi ion
- Phản ứng bay hơi dung dịch muối
- Phân hủy một số hợp chất
Phân loại muối
Muối có thể được phân loại theo nhiều tiêu chí khác nhau, hai cách phổ biến nhất là dựa trên loại cation và loại anion:
- Phân loại theo loại cation:
- Muối kim loại: Là loại muối được tạo thành từ cation kim loại và anion gốc axit. Ví dụ: muối natri (NaCl), muối kali (KCl), muối canxi (CaCl2),…
- Muối amoni: Là loại muối được tạo thành từ cation amoni (NH4+) và anion gốc axit. Ví dụ: muối amoni sunfat ((NH4)2SO4), muối amoni nitrat (NH4NO3),…
- Phân loại theo loại anion:
- Muối halogenua: Là loại muối được tạo thành từ cation kim loại và anion halogen (F-, Cl-, Br-, I-). Ví dụ: muối natri clorua (NaCl), muối kali bromua (KBr),…
- Muối sunfat: Là loại muối được tạo thành từ cation kim loại và anion sunfat (SO42-). Ví dụ: muối canxi sunfat (CaSO4), muối natri sunfat (Na2SO4),…
- Muối nitrat: Là loại muối được tạo thành từ cation kim loại và anion nitrat (NO3-). Ví dụ: muối kali nitrat (KNO3), muối bạc nitrat (AgNO3),…
Cách đặt tên muối:
Tên của muối được đặt dựa trên tên của cation và anion theo thứ tự sau:
- Tên cation: Sử dụng tên tiếng Việt của cation kim loại hoặc tên amoni. Ví dụ: natri, kali, canxi, amoni,…
- Tên anion: Thay đổi đuôi “-ua” thành “-it” đối với các anion có nhiều hóa trị. Ví dụ: clorua (Cl-), sunfat (SO42-), nitrat (NO3-),… Đối với anion có hóa trị 1, giữ nguyên đuôi “-ua”. Ví dụ: florua (F-), bromua (Br-), iotua (I-).
- Số lượng nguyên tử của mỗi nguyên tố (nếu nhiều hơn 1): Ghi số lượng nguyên tử của mỗi nguyên tố bằng chữ số La Mã đặt trước tên anion. Ví dụ: natri sunfat (Na2SO4), canxi nitrat (Ca(NO3)2),…
Ví dụ:
- Natri clorua (NaCl): Natri (cation) + clorua (anion)
- Kali sunfat (K2SO4): Kali (cation) + sunfat (anion) với 2 nguyên tử kali
- Canxi dihiđrophotphat (CaH2PO4): Canxi (cation) + dihiđrophotphat (anion)
Tính chất của muối
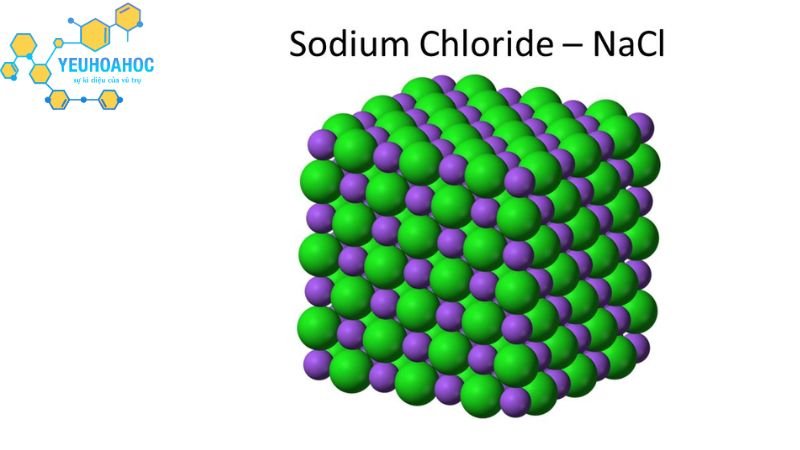
Tính chất vật lý của muối
Muối có nhiều tính chất vật lý khác nhau, tùy thuộc vào loại muối cụ thể. Sau đây là một số tính chất vật lý phổ biến của muối:
Trạng thái
- Hầu hết các muối ở trạng thái rắn ở nhiệt độ phòng, dạng tinh thể.
- Một số ít muối ở dạng lỏng, ví dụ như natri clorua nóng chảy.
- Một số ít muối khác ở dạng khí, ví dụ như amoniac clorua.
Màu sắc
- Muối thường có màu trắng.
- Một số muối có màu đặc trưng do sự hiện diện của các ion kim loại, ví dụ như:
- Muối đồng sunfat (CuSO4) có màu xanh lam.
- Muối sắt(III) clorua (FeCl3) có màu vàng nâu.
- Muối kali permanganat (KMnO4) có màu tím.
Độ tan trong nước
- Muối có độ tan trong nước khác nhau.
- Một số muối tan rất tốt trong nước, ví dụ như natri clorua (NaCl), kali clorua (KCl).
- Một số muối ít tan trong nước, ví dụ như canxi sunfat (CaSO4), bạc clorua (AgCl).
- Một số muối không tan trong nước, ví dụ như bari sunfat (BaSO4), chì sunfat (PbSO4).
Điểm nóng chảy và điểm sôi
- Muối là chất có điểm nóng chảy và điểm sôi cao.
- Điểm nóng chảy và điểm sôi của muối phụ thuộc vào cấu trúc tinh thể và lực hút tĩnh điện giữa các ion.
Khối lượng riêng
- Khối lượng riêng của muối cũng khác nhau.
- Khối lượng riêng của muối thường dao động từ 1 g/cm³ đến 5 g/cm³.
Ví dụ:
| Muối | Trạng thái | Màu sắc | Độ tan trong nước | Điểm nóng chảy (°C) | Điểm sôi (°C) | Khối lượng riêng (g/cm³) |
| Natri clorua (NaCl) | Rắn | Trắng | Rất tan | 801 | 1461 | 2.16 |
| Kali clorua (KCl) | Rắn | Trắng | Rất tan | 770 | 1500 | 1.96 |
| Canxi sunfat (CaSO4) | Rắn | Trắng | Ít tan | 1430 | 2462 | 2.33 |
| Bạc clorua (AgCl) | Rắn | Trắng | Không tan | 455 | 1500 | 5.63 |
Tính chất hóa học của muối
Muối có nhiều tính chất hóa học quan trọng, bao gồm:
- Phản ứng phân hủy:
- Một số muối bị phân hủy ở nhiệt độ cao, thu được kim loại và khí hoặc oxit kim loại. Ví dụ:
- Phản ứng phân hủy muối thường tỏa nhiệt.
- Phản ứng trung hòa axit – bazơ:
- Muối có thể tác dụng với axit hoặc bazơ để tạo thành muối mới và nước. Ví dụ:
- Phản ứng trung hòa axit – bazơ thường tỏa nhiệt.
- Phản ứng trao đổi ion:
- Hai dung dịch muối có thể tác dụng với nhau để tạo thành hai muối mới, nếu có ít nhất một cặp ion chung. Ví dụ:
- Phản ứng trao đổi ion xảy ra khi tích điện của dung dịch thu được bằng 0.
- Một số tính chất đặc trưng khác:
- Muối tan trong nước tạo dung dịch dẫn điện.
- Muối có vị mặn, một số muối có vị ngọt hoặc đắng.
- Muối có thể kết tinh từ dung dịch.
Ví dụ về một số muối có tính chất đặc trưng:
- Muối ăn (NaCl): có vị mặn, tan tốt trong nước, dễ hút ẩm, được sử dụng trong đời sống và công nghiệp.
- Canxi sunfat (CaSO4): ít tan trong nước, được sử dụng trong sản xuất thạch cao, xi măng.
- Kali nitrat (KNO3): dễ tan trong nước, được sử dụng làm phân bón, thuốc nổ.
- Natri cacbonat (Na2CO3): có tính bazơ yếu, được sử dụng trong sản xuất xà phòng, thủy tinh.
- Bạc clorua (AgCl): không tan trong nước, có màu trắng, được sử dụng trong chụp ảnh.
Ứng dụng của muối
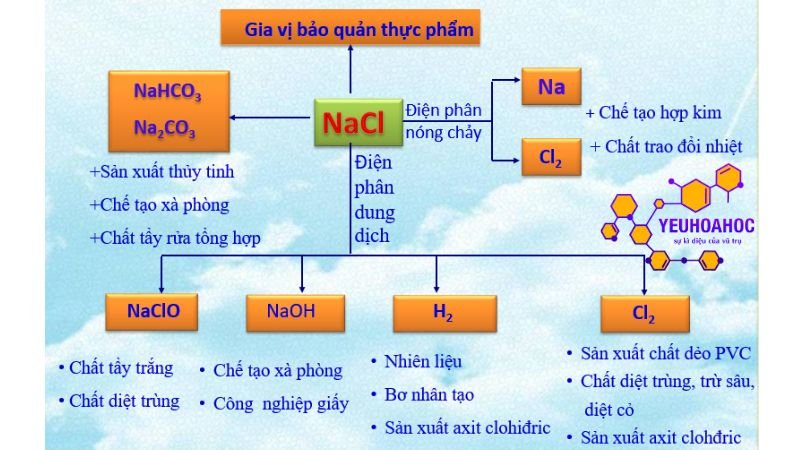
Ứng dụng trong ẩm thực:
- Gia vị: Muối là gia vị cơ bản không thể thiếu trong gian bếp, giúp nêm nếm và tăng hương vị cho món ăn.
- Bảo quản thực phẩm: Muối có khả năng hút nước, ức chế vi khuẩn, do đó được sử dụng để bảo quản thực phẩm như thịt, cá, rau củ quả,…
- Ứng dụng trong y học:
- Dung dịch muối sinh lý: Dùng để rửa mắt, mũi, họng, sát trùng vết thương, tiêm truyền, v.v.
- Thuốc sát trùng: Muối có tính sát khuẩn nhẹ, được sử dụng trong dung dịch vệ sinh răng miệng, khử trùng dụng cụ y tế.
- Điều trị một số bệnh lý: Nước muối có thể giúp giảm nghẹt mũi, loét miệng, tiêu chảy, v.v.
- Ứng dụng trong công nghiệp:
- Sản xuất hóa chất: Muối là nguyên liệu cho nhiều hóa chất quan trọng như Clo, NaOH, axit Clohydric,…
- Sản xuất xà phòng, chất tẩy rửa: Muối được sử dụng trong sản xuất xà phòng, chất tẩy rửa, giúp tăng độ cứng và tạo bọt.
- Công nghiệp lạnh: Muối được dùng trong dung dịch nước muối để làm lạnh, bảo quản thực phẩm, sản xuất đá viên.
- Ứng dụng trong nông nghiệp:
- Phân bón: Cung cấp Natri và Clo cho cây trồng, giúp tăng năng suất và chất lượng.
- Diệt trừ sâu bệnh: Một số loại muối có thể được sử dụng để diệt trừ một số loại sâu bệnh hại cây trồng.
Ngoài ra, muối còn có nhiều ứng dụng khác trong đời sống như:
- Làm đẹp: Tẩy tế bào chết, dưỡng da, trị mụn,…
- Dọn dẹp nhà cửa: Khử mùi hôi, tẩy rửa vết bẩn,…
- Làm thủ công: Làm muối tắm, nến thơm,…
Điều chế và sản xuất muối
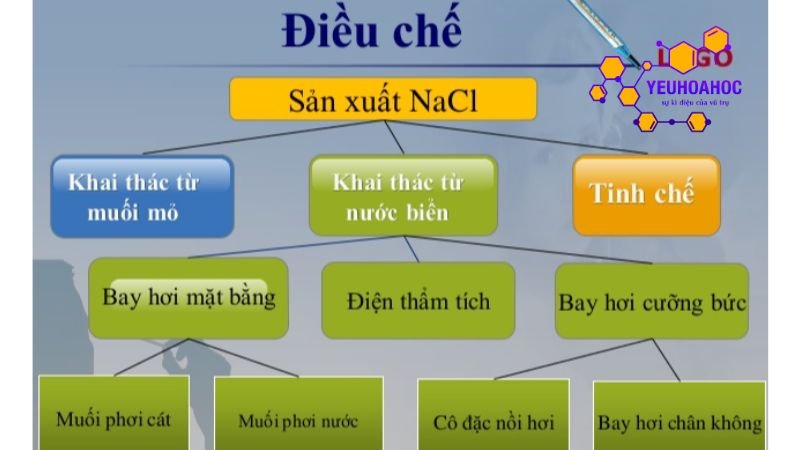
Muối, hay Natri Clorua (NaCl), là một hợp chất hóa học phổ biến được sử dụng rộng rãi trong đời sống. Việc điều chế và sản xuất muối có thể được thực hiện theo hai phương pháp chính:
Trong công nghiệp
Phương pháp phơi nắng: Đây là phương pháp truyền thống được sử dụng phổ biến nhất ở Việt Nam và nhiều nơi trên thế giới. Quy trình cơ bản bao gồm:
- Lấy nước biển: Nước biển được lấy từ vùng ven biển, sau đó dẫn vào các ruộng muối.
- Làm bay hơi nước: Nước biển được phơi nắng để nước bay hơi, dần dần làm tăng nồng độ muối.
- Thu hoạch muối: Khi nồng độ muối đạt đến mức bão hòa, muối sẽ kết tinh và được thu hoạch bằng tay hoặc máy móc.
Phương pháp cô đặc: Phương pháp này sử dụng nhiệt để làm bay hơi nước biển, giúp rút ngắn thời gian sản xuất và tăng năng suất. Quy trình gồm các bước:
- Lọc nước biển: Nước biển được lọc để loại bỏ tạp chất.
- Cô đặc: Nước biển được cô đặc bằng cách đun sôi trong nồi hoặc sử dụng thiết bị bay hơi.
- Kết tinh: Khi nồng độ muối đạt đến mức bão hòa, muối sẽ kết tinh và được thu hoạch.
Trong phòng thí nghiệm
Phương pháp kết tinh:
- Pha dung dịch NaCl: Hòa tan NaCl tinh khiết vào nước cất để tạo thành dung dịch bão hòa.
- Làm nguội dung dịch: Dung dịch NaCl được làm nguội dần để thúc đẩy quá trình kết tinh.
- Lọc và thu hoạch: Muối kết tinh sẽ lắng xuống đáy bình, sau đó được lọc và thu hoạch.
Phương pháp điện phân:
- Pha dung dịch NaCl: Hòa tan NaCl tinh khiết vào nước cất.
- Điện phân dung dịch: Dòng điện được truyền qua dung dịch NaCl, tách NaCl thành Na và Cl ở hai điện cực.
- Thu hoạch NaCl: Na được thu gom ở điện cực âm, Cl được thu gom ở điện cực dương. Sau đó, Na và Cl được kết hợp lại để tạo thành NaCl.
Tác hại của việc sử dụng muối quá mức
Ảnh hưởng đến sức khỏe:
- Tăng huyết áp: Muối có chứa natri, một nguyên tố có thể làm tăng lượng nước trong máu, dẫn đến tăng áp lực lên thành mạch máu và tim, gây ra bệnh cao huyết áp. Huyết áp cao là yếu tố nguy cơ chính dẫn đến các bệnh tim mạch nguy hiểm như nhồi máu cơ tim, đột quỵ.
- Sỏi thận: Natri trong muối dư thừa có thể kết hợp với các khoáng chất khác trong cơ thể, tạo thành sỏi thận. Sỏi thận có thể gây ra đau đớn dữ dội, nhiễm trùng đường tiết niệu và thậm chí suy thận.
- Bệnh tim mạch: Huyết áp cao do ăn nhiều muối có thể dẫn đến các vấn đề tim mạch khác như suy tim, nhồi máu cơ tim và đột quỵ.
- Ung thư dạ dày: Một số nghiên cứu cho thấy ăn nhiều muối có thể làm tăng nguy cơ mắc bệnh ung thư dạ dày.
- Loãng xương: Ăn nhiều muối có thể làm tăng lượng canxi bài tiết qua nước tiểu, dẫn đến loãng xương, làm tăng nguy cơ gãy xương.
- Gây phù nề: Ăn nhiều muối có thể khiến cơ thể giữ nước nhiều hơn, dẫn đến phù nề, đặc biệt là ở mặt, tay và chân.
Gây ô nhiễm môi trường:
- Xâm nhập nước và đất: Muối dư thừa từ các hoạt động nông nghiệp, công nghiệp và sinh hoạt có thể xâm nhập vào nguồn nước và đất, ảnh hưởng đến chất lượng nước uống và gây hại cho các sinh vật sống trong môi trường.
- Gây hại cho hệ sinh thái: Muối có thể làm thay đổi độ pH của đất và nước, ảnh hưởng đến sự phát triển của các loài thực vật và động vật. Nước mặn có thể xâm nhập vào đất liền, làm chết các cây trồng và phá hủy hệ sinh thái ven biển.
Giải pháp hạn chế tác hại của việc sử dụng muối quá mức:
- Giảm lượng muối tiêu thụ: Theo khuyến cáo của Tổ chức Y tế Thế giới (WHO), mỗi người trưởng thành chỉ nên tiêu thụ tối đa 5g muối mỗi ngày.
- Hạn chế sử dụng các thực phẩm chế biến sẵn: Các thực phẩm chế biến sẵn thường chứa nhiều muối, do đó, nên hạn chế sử dụng để bảo vệ sức khỏe.
- Đọc kỹ nhãn thực phẩm: Khi mua thực phẩm, hãy đọc kỹ nhãn để biết hàm lượng muối trong sản phẩm và chọn những sản phẩm có hàm lượng muối thấp.
- Sử dụng các loại gia vị khác: Thay vì chỉ sử dụng muối để nêm nếm thức ăn, hãy thử sử dụng các loại gia vị khác như thảo mộc, ớt, tiêu,… để tăng thêm hương vị cho món ăn mà không cần thêm nhiều muối.
- Nâng cao nhận thức: Cần nâng cao nhận thức của cộng đồng về tác hại của việc sử dụng muối quá mức và khuyến khích mọi người thực hành lối sống lành mạnh, hạn chế tiêu thụ muối để bảo vệ sức khỏe và môi trường.
Hành trình khám phá muối vẫn còn nhiều điều bí ẩn chờ đợi được giải mã. Hãy cùng trân trọng nguồn tài nguyên thiên nhiên quý giá này, sử dụng muối một cách thông minh và góp phần bảo vệ môi trường.









