Trong vô số nguyên tố hóa học đã được khám phá và nghiên cứu, Tennessine nổi bật như một phát hiện đáng chú ý nhất trong thời gian gần đây. Với số hiệu nguyên tử 117, Tennessine không chỉ là một nguyên tố phóng xạ và siêu nặng mà còn mang theo câu chuyện hình thành đầy thú vị của mình. Bài viết này, yeuhoahoc.edu.vn sẽ đưa bạn vào hành trình khám phá nguyên tố Tennessine – từ định nghĩa, lịch sử phát hiện, đến vị trí của nó trong bảng tuần hoàn hóa học.
Giới thiệu về nguyên tố Tennessine
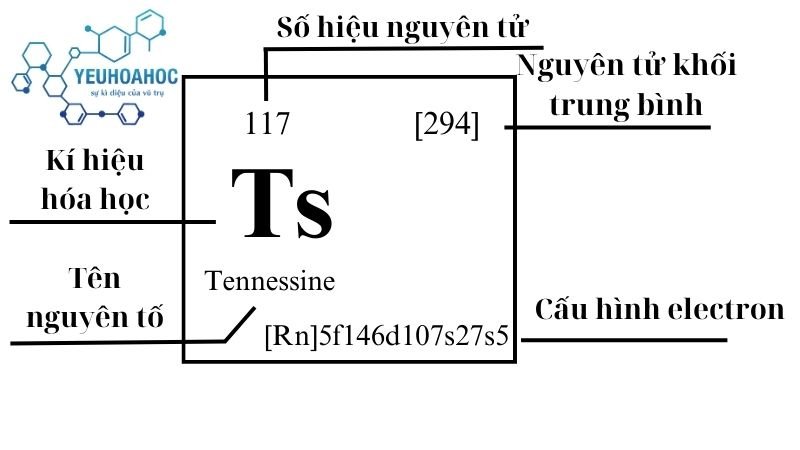
Định nghĩa
Tennessine, với tên tiếng Anh là “Tennessine” và kí hiệu là “Ts”, là một nguyên tố hóa học nhân tạo, phóng xạ, với số hiệu nguyên tử là 117. Nó thuộc nhóm các nguyên tố siêu nặng trong bảng tuần hoàn và được tạo ra thông qua các phản ứng hạt nhân đặc biệt trong phòng thí nghiệm.
Lịch sử hình thành Tennessine
- 2004: Nhóm nghiên cứu tại Phòng thí nghiệm Quốc gia Oak Ridge (ORNL) và Đại học Vanderbilt (VU) bắt đầu nghiên cứu tổng hợp Tennessine.
- 2009: Tháng 4, nhóm nghiên cứu ORNL/VU thông báo đã tổng hợp thành công Tennessine.
- 2010: Tháng 6, IUPAC công nhận việc phát hiện Tennessine.
- 2016: Tennessine được đặt tên theo bang Tennessee, nơi ORNL và VU tọa lạc.
Mốc thời gian quan trọng:
- 2004: Bắt đầu nghiên cứu tổng hợp Tennessine.
- 2009: Tổng hợp thành công Tennessine.
- 2010: IUPAC công nhận việc phát hiện Tennessine.
- 2016: Tennessine được đặt tên theo bang Tennessee.
Nguyên tố Tennessine trong bảng tuần hoàn hóa học
- Thuộc nhóm 17 (Halogen) trong bảng tuần hoàn.
- Là nguyên tố nhân tạo, không có trong tự nhiên.
- Có tính phóng xạ cao, phân rã thành các nguyên tố nhẹ hơn.
| Nhóm | Chu kỳ | Nguyên tử khối (u) | Khối lượng riêng g/cm3 | Nhiệt độ nóng chảy (K) | Nhiệt độ bay hơi
K |
Nhiệt dung riêng
J/gK |
Độ âm điện | Tỷ lệ trong vỏ Trái Đất
mg/kg |
| 17 | 7 | [294] | (7,2) | (673) | (823) | – | – | 0 |
Tính chất của nguyên tố Tennessine
Tính chất vật lý
- Do là nguyên tố nhân tạo, Tennessine chỉ được tổng hợp với số lượng rất ít (chỉ 6 nguyên tử) nên các tính chất vật lý của nó chưa được nghiên cứu đầy đủ.
- Dự đoán:
- Là kim loại nặng, có màu trắng bạc.
- Nhiệt độ nóng chảy và sôi cao.
- Khối lượng riêng cao.
Tính chất hóa học
- Thuộc nhóm 17 (Halogen) trong bảng tuần hoàn.
- Dự đoán:
- Có tính oxi hóa mạnh.
- Có khả năng kết hợp tạo thành hợp chất với các loại kim loại khác.
- Có thể tạo thành ion Ts-.
Ứng dụng của nguyên tố Tennessine

Hiện nay, Tennessine chỉ được sử dụng trong nghiên cứu khoa học, cụ thể là:
- Nghiên cứu cấu tạo hạt nhân nguyên tử: Tennessine giúp các nhà khoa học hiểu rõ hơn về cấu tạo và hoạt động của hạt nhân nguyên tử, từ đó có thể phát triển các công nghệ mới trong lĩnh vực năng lượng hạt nhân.
- Nghiên cứu tổng hợp các nguyên tố mới: Tennessine là bước đệm quan trọng trong việc tổng hợp các nguyên tố mới nặng hơn, mở rộng bảng tuần hoàn hóa học.
- Ứng dụng trong y học hạt nhân: Trong tương lai, Tennessine có thể được sử dụng trong y học hạt nhân để chẩn đoán và điều trị ung thư.
Tuy nhiên, do Tennessine có tính phóng xạ cao và chỉ được tổng hợp với số lượng rất ít, nên việc ứng dụng nó trong thực tế còn gặp nhiều hạn chế. Các nhà khoa học đang nghiên cứu để tìm ra các phương pháp tổng hợp Tennessine hiệu quả hơn và giảm thiểu nguy cơ phóng xạ của nó.
Dưới đây là một số tiềm năng ứng dụng của Tennessine trong tương lai:
- Chẩn đoán ung thư: Tennessine có thể được sử dụng để tạo ra các chất đánh dấu phóng xạ giúp chẩn đoán ung thư chính xác hơn.
- Điều trị ung thư: Tennessine có thể được sử dụng để tạo ra các loại thuốc điều trị ung thư mới hiệu quả hơn.
- Xạ trị: Tennessine có thể được sử dụng để tạo ra các nguồn bức xạ mạnh để điều trị ung thư.
Điều chế và sản xuất nguyên tố Tennessine
Điều chế
Điều chế trong phòng thí nghiệm:
Tennessine được điều chế lần đầu tiên vào năm 2010 tại Phòng thí nghiệm quốc gia Oak Ridge (ORNL) ở Tennessee, Hoa Kỳ. Nhóm nghiên cứu do Giáo sư Thomas D. Glasmacher dẫn đầu đã bắn phá một mục tiêu bismuth-209 bằng chùm hạt nhân berkelium-48. Phản ứng này tạo ra một hạt nhân tennessine-257, phân rã thành một hạt alpha và một hạt nhân polonium-253.
Phương trình điều chế:
^209Bi + ^48Bk → ^257Ts → ^4He + ^253Po
Điều chế trong công nghiệp:
Hiện nay, Tennessine không được sản xuất trong công nghiệp. Việc điều chế nguyên tố Tennessine rất tốn kém và phức tạp, chỉ được thực hiện trong các phòng thí nghiệm nghiên cứu.
Sản xuất
Nguyên tố Tennessine không có ứng dụng thực tế nào được biết đến. Do tính phóng xạ cao, nó chỉ được sử dụng trong nghiên cứu khoa học.
Lưu ý:
Tennessine là một nguyên tố hóa học nhân tạo, không có trong tự nhiên. Nó là nguyên tố có số nguyên tử 117, được đặt tên theo bang Tennessee của Hoa Kỳ, nơi nó được điều chế lần đầu tiên.
Phản ứng hóa học của nguyên tố Tennessine

Phản ứng phân rã
Tennessine không bền và phân rã thành các nguyên tố khác. Ví dụ:
- Tennessine-257 phân rã thành alpha và polonium-253:
^257Ts → ^4He + ^253Po
- Tennessine-261 phân rã thành alpha và polonium-257:
^261Ts → ^4He + ^257Po
Phản ứng oxy hóa khử
Tennessine có thể thể hiện các trạng thái oxy hóa +1, +3 và +5 trong các hợp chất. Ví dụ:
- Tennessine(I) chloride (TsCl): Tennessine thể hiện trạng thái oxy hóa +1 trong hợp chất này.
- Tennessine(III) chloride (TsCl3): Tennessine thể hiện trạng thái oxy hóa +3 trong hợp chất này.
- Tennessine(V) fluoride (TsF5): Tennessine thể hiện trạng thái oxy hóa +5 trong hợp chất này.
Phản ứng với axit và bazơ
Tennessine có thể phản ứng với axit và bazơ để tạo thành muối. Ví dụ:
- Tennessine hydroxide (TsOH): Tennessine phản ứng với nước để tạo thành hydroxide.
- Tennessine carbonate (TsCO3): Tennessine phản ứng với axit cacbonic để tạo thành carbonate.
Phản ứng với phối tử
Tennessine có thể tạo thành các phức chất với các phối tử như EDTA và pyridine.
Ví dụ cụ thể:
- Nhóm nghiên cứu tại Đại học Mainz (Đức) đã nghiên cứu phản ứng của tennessine-261 với axit nitric. Họ phát hiện ra rằng tennessine-261 bị oxy hóa thành tennessine(V) và tạo thành nitrat tennessine(V).
^261Ts + 6HNO3 → ^261Ts(NO3)5 + 3H2O + 3NO2
- Nhóm nghiên cứu tại Phòng thí nghiệm quốc gia Oak Ridge (ORNL) đã nghiên cứu phản ứng của tennessine-257 với khí hydro chloride. Họ phát hiện ra rằng tennessine-257 bị khử thành tennessine(I) và tạo thành chloride tennessine(I).
^257Ts + HCl → ^257TsCl + H2
Vấn đề an toàn của nguyên tố Tennessine
Tennessine là một nguyên tố nhân tạo có tính phóng xạ cao, do đó nó tiềm ẩn nhiều nguy cơ về an toàn:
Nguy cơ bức xạ:
- Tennessine phát ra tia alpha và beta, có thể gây tổn thương tế bào và DNA.
- Tiếp xúc với tennessine có thể dẫn đến các bệnh ung thư, đột biến gen và các vấn đề sức khỏe khác.
Nguy cơ ô nhiễm môi trường:
- Tennessine có thể xâm nhập vào môi trường thông qua các hoạt động nghiên cứu hoặc tai nạn.
- Ô nhiễm tennessine có thể gây hại cho hệ sinh thái và con người.
Nguy cơ khủng bố:
- Tennessine có thể được sử dụng để chế tạo vũ khí hạt nhân hoặc bẩn.
- Việc sử dụng tennessine cho mục đích khủng bố có thể gây ra hậu quả thảm khốc.
Để đảm bảo an toàn, khi tiếp xúc với nguyên tố tennessine cần thực hiện các biện pháp sau:
- Kiểm soát chặt chẽ việc sản xuất và sử dụng tennessine:
- Chỉ cho phép các nhà khoa học có trình độ và kinh nghiệm sử dụng tennessine.
- Áp dụng các biện pháp an toàn nghiêm ngặt để ngăn ngừa rò rỉ tennessine ra môi trường.
- Nghiên cứu và phát triển các phương pháp xử lý tennessine an toàn:
- Phát triển các phương pháp để loại bỏ tennessine khỏi môi trường.
- Phát triển các phương pháp để điều trị các bệnh do tiếp xúc với tennessine.
- Nâng cao nhận thức về nguy cơ của tennessine:
- Nâng cao nhận thức của cộng đồng về nguy cơ của tennessine.
- Đào tạo cho các nhân viên y tế và ứng phó khẩn cấp về cách xử lý các trường hợp khẩn cấp liên quan đến tennessine.
Kết thúc bài viết, chúng ta đã cùng nhau khám phá những thông tin thú vị và quan trọng về nguyên tố tennessine, mở ra cánh cửa kiến thức rộng lớn trong lĩnh vực hóa học. Tại yeuhoahoc.edu.vn, chúng tôi luôn cam kết cung cấp nội dung chất lượng cao, cập nhật và dễ hiểu, giúp bạn dễ dàng tiếp cận và yêu thích môn học này hơn. Đừng quên theo dõi chúng tôi để cập nhật những thông tin mới nhất và sâu sắc nhất về hóa học. Hãy cùng chúng tôi tiếp tục hành trình khám phá thế giới hóa học đầy màu sắc và bí ẩn!









